
| A. | Na2S和AlCl3 | B. | 乙烷与乙烯 | C. | 直馏汽油与苯 | D. | CO2与SO2 |
分析 能与酸性高锰酸钾溶液发生氧化还原反应的有机物有不饱和烃、苯的同系物、醛、醇、Na2S、SO2等,以此解答该题.
解答 解:A.Na2S与高锰酸钾发生氧化还原反应使其褪色,AlCl3不能,现象不同,可鉴别,故A不选;
B.乙烯与高锰酸钾发生氧化还原反应使其褪色,乙烷不能,现象不同,可鉴别,故B不选;
C.二者与高锰酸钾均不反应,分层后有机层均在上层,现象相同,不能鉴别,故C选;
D.SO2与高锰酸钾发生氧化还原反应使其褪色,CO2不能,现象不同,可鉴别,故D不选;
故选C.
点评 本题考查物质的鉴别,为高频考点,注意把握有机物的性质的异同,归纳常见能与酸性高锰酸钾反应的有机物的种类及还原性物质,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铝片和稀盐酸反应 | B. | Ba(OH)2•8H2O与NH4Cl的反应 | ||
| C. | 酒精在氧气中的燃烧 | D. | 灼热的碳与水蒸汽的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
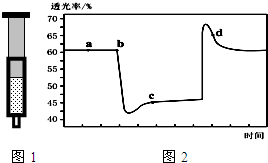 已知反应:2NO2 (红棕色)?N2O4(无色)△H<0.将一定量的NO2充入注射器中后封口,图1和图2是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )
已知反应:2NO2 (红棕色)?N2O4(无色)△H<0.将一定量的NO2充入注射器中后封口,图1和图2是在拉伸和压缩注射器的过程中气体透光率随时间的变化(气体颜色越深,透光率越小).下列说法正确的是( )| A. | b点的操作是拉伸注射器 | |
| B. | d 点:v(正)<v(逆) | |
| C. | c点与a点相比,c(NO2)增大,c(N2O4)减小 | |
| D. | 若不忽略体系温度变化,且没有能量损失,则T(b)>T(c) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 每一个水分子内平均含有两个氢键 | |
| B. | 氢键与配位键一样,也是共价键的一种 | |
| C. | 氢键是导致浓硫酸具有粘稠性原因之一 | |
| D. | 由于H2O中含有氢键,因此水是一种非常稳定的化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直线 sp杂化 | B. | V型 sp2杂化 | ||
| C. | 三角锥形 sp3杂化 | D. | 平面三角形 sp2 杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,10mL 0.50mol•L-1NH4Cl溶液与20mL 0.25mol•L-1NH4C1溶液含NH4+物质的量相同 | |
| B. | 25℃时,将a mo1•L-l氨水与0.01 moI•L-1盐酸等体积混合,反应完全时溶液中c(NH4+)=c(C1-),用含a的代数式表示反应完全时NH3•H2O的电离常数Kb=$\frac{1{0}^{-9}}{a-0.01}$ | |
| C. | 一定温度下,已知0.1 mol•L-1 的醋酸溶液中存在电离平衡:CH3COOH?CH3COO-+H+,加少量烧碱溶液可使溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$值增大 | |
| D. | 等体积、pH都为3的酸HA和HB分别与足量的锌反应,HA放出的氢气多,说明酸性:HA>HB |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:K+>Mg2+>Na+ | |
| B. | 热稳定性:NaHCO3>Na2CO3>H2CO3 | |
| C. | 结合H+的能力:OH->ClO->HCO3- | |
| D. | 相同pH的HCl和CH3COOH加水稀释相同倍数,pH:CH3COOH>HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| n(SO32-):n(HSO3-) | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 阴、阳离子之间通过相互吸引作用形成的化学键叫离子键 | |
| B. | 根据电离方程式HCl=H++Cl-,可判断HC1分子里存在离子键 | |
| C. | 化学键的断裂和形成是化学反应能量变化的主要原因 | |
| D. | 离子化合物一定由金属元素和非金属元素组成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com