
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:高中化学 来源:不详 题型:单选题
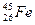 原子,有关
原子,有关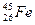 的说法正确的是( )
的说法正确的是( )| A.它是一种新元素 | B.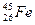 与 与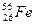 互为同素异形体 互为同素异形体 |
| C.它是一种新核素 | D.这是铁原子发生衰变放出两个质子形成的核素 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素代号 | A | B | D | E | G | H | I | J |
| 常见化合价 | -1 | -2 | +4、-4 | +6、+4、-2 | +5、-3 | +3 | +2 | +1 |
| 原子半径/pm | 64 | 66 | 77 | 104 | 110 | 143 | 160 | 186 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1S22S22P63S23P64S 1与1S22S22P63S1 |
| B.1S22S22P63S2与1S22S22P63S23P1 |
| C.1S22S22P63S23P4与1S22S22P6 |
| D.1S22S22P2与1S22S22P5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.X元素能形成+7价的含氧酸及其盐 |
| B.Y元素原子核最外层电子数为2 |
| C.Z元素的阴离子与同一周期惰性元素的原子结构相同 |
| D.R元素的氧化物是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属性逐渐增强 |
| B.离子的氧化性逐渐减小 |
| C.金属的熔点逐渐升高 |
| D.原子半径逐渐减小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知Ra是第7周期、ⅡA族的元素,故Ra(OH)2的碱性比Mg(OH)2的碱性强 |
| B.已知As是第4周期、ⅤA族的元素,故AsH3的稳定性比NH3的稳定性强 |
| C.已知Cs的原子半径比Na的大,故Cs与水反应比Na与水反应更剧烈 |
| D.已知Cl的核电荷数比Al的核电荷数大,故 Cl的原子半径比Al的原子半径小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com