
 ��ѧ-ѡ���л���ѧ����
��ѧ-ѡ���л���ѧ����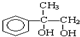 ���
���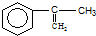 �����ϳ�A��
�����ϳ�A��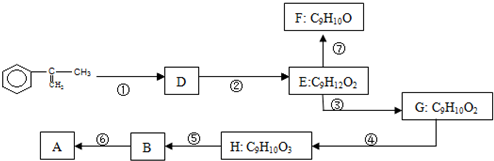
| HBr |
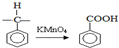
 ��A����������ˮ������B��״�����BΪ
��A����������ˮ������B��״�����BΪ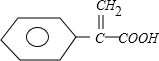 ��E�ĽṹʽΪ
��E�ĽṹʽΪ ��E��Ӧ����F��F�ķ���ʽΪC9H10O����E��ȼ���1����H2O�����ϩ��ʽ���ȶ�����ת��Ϊȩ����FΪ
��E��Ӧ����F��F�ķ���ʽΪC9H10O����E��ȼ���1����H2O�����ϩ��ʽ���ȶ�����ת��Ϊȩ����FΪ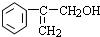 ��
��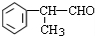 ��
��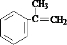 ��Ӧ����D��D��ת������E
��Ӧ����D��D��ת������E ��ת������������2��-OH����
��ת������������2��-OH���� Ӧ�����巢���ӳɷ�ӦD��D������������ˮ��Һ�����������·���ˮ�ⷴӦ����DΪ
Ӧ�����巢���ӳɷ�ӦD��D������������ˮ��Һ�����������·���ˮ�ⷴӦ����DΪ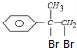 ��Eת������G��E�����м���2��Hԭ������G����Ϊ-OH��������-CHO����GΪ
��Eת������G��E�����м���2��Hԭ������G����Ϊ-OH��������-CHO����GΪ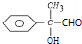 ��Gת������H��G��������1��Oԭ������H��Ϊ-CHO����Ϊ-COOH����HΪ
��Gת������H��G��������1��Oԭ������H��Ϊ-CHO����Ϊ-COOH����HΪ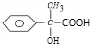 ��H������ȥ��Ӧ����F���ݴ˽��
��H������ȥ��Ӧ����F���ݴ˽�� ��A����������ˮ������B��״�����BΪ
��A����������ˮ������B��״�����BΪ ��E�ĽṹʽΪ
��E�ĽṹʽΪ ��E��Ӧ����F��F�ķ���ʽΪC9H10O����E��ȼ���1����H2O����FΪ
��E��Ӧ����F��F�ķ���ʽΪC9H10O����E��ȼ���1����H2O����FΪ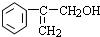 ��
��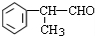 ��
�� ��Ӧ����D��D��ת������E
��Ӧ����D��D��ת������E ��ת������������2��-OH����
��ת������������2��-OH���� Ӧ�����巢���ӳɷ�ӦD��D������������ˮ��Һ�����������·���ˮ�ⷴӦ����DΪ
Ӧ�����巢���ӳɷ�ӦD��D������������ˮ��Һ�����������·���ˮ�ⷴӦ����DΪ ��Eת������G��E�����м���2��Hԭ������G����Ϊ-OH��������-CHO����GΪ
��Eת������G��E�����м���2��Hԭ������G����Ϊ-OH��������-CHO����GΪ ��Gת������H��G��������1��Oԭ������H��Ϊ-CHO����Ϊ-COOH����HΪ
��Gת������H��G��������1��Oԭ������H��Ϊ-CHO����Ϊ-COOH����HΪ ��H������ȥ��Ӧ����F��
��H������ȥ��Ӧ����F�� ����������ˮ��Һ�����������·���ˮ�ⷴӦ����
����������ˮ��Һ�����������·���ˮ�ⷴӦ���� ��
�� ��Cu��������������������Ӧ����
��Cu��������������������Ӧ���� ��
�� ��Ũ���ᡢ���������·�����ȥ��Ӧ����
��Ũ���ᡢ���������·�����ȥ��Ӧ���� ��
�� ��DΪ
��DΪ ��GΪ
��GΪ ��
�� ��
�� ��
�� ��
��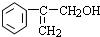 ��
��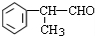 ����������������Һ[������Cu��OH��2����Һ]��������
����������������Һ[������Cu��OH��2����Һ]��������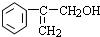 ��
��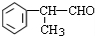 ��������Һ[������Cu��OH��2����Һ]��
��������Һ[������Cu��OH��2����Һ]��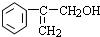 ����HBr�����ӳɷ�Ӧ����ֹC=C����������Cu�����������½�-OH����Ϊ-CHO��������������ͭ�����������½�һ����-CHO����Ϊ-COOH��������������ƴ���Һ�����������·�����ȥ��Ӧ�����ữ�Ƶ�
����HBr�����ӳɷ�Ӧ����ֹC=C����������Cu�����������½�-OH����Ϊ-CHO��������������ͭ�����������½�һ����-CHO����Ϊ-COOH��������������ƴ���Һ�����������·�����ȥ��Ӧ�����ữ�Ƶ� ����F1�ϳ�B������ͼΪ��
����F1�ϳ�B������ͼΪ��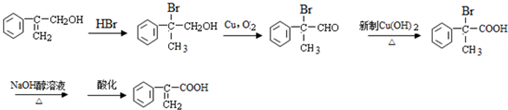 ��
�� ��
��


 ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Fe3+��H+��ClO-��SO32- |
| B��K+��Al3+��Cl-��CO32- |
| C��Na+��Ca2+��HCO3-��OH- |
| D��Al3+��NH4+��Cl-��SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Na2O+H2O�T2NaOH | ||||
| B��2F2+2H2O�T4HF+O2 | ||||
| C��Cl2+H2O�THCl+HClO | ||||
D��2H2O
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����״���£�5.6 L NO��5.6 L O2��Ϻ�ķ�������Ϊ0.5 NA |
| B��1 mol������Ӻ���8 NA�����ۼ� |
| C��58.5 g�Ȼ��ƹ����к���NA���Ȼ��Ʒ��� |
| D����1 L 0.1 mol/L̼������Һ��������������0.1 NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | 5 |
| c��NO����mol/L�� | 1.00��10-3 | 4.50��10-4 | 2.50��10-4 | 1.50��10-4 | 1.00��10-4 | 1.00��10-4 |
| c��CO����mol/L�� | 3.60��10-3 | 3.05��10-3 | 2.85��10-3 | 2.75��10-3 | 2.70��10-3 | 2.70��10-3 |
| ʵ�� ��� |
T���棩 | NO��ʼŨ�� ��mol/L�� |
CO��ʼŨ�� ��mol/L�� |
�����ıȱ������m2/g�� |
| �� | 280 | 1.20��10-3 | 5.80��10-3 | 82 |
| �� | 124 | |||
| �� | 350 | 124 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||||
B��
| ||||
C��
| ||||
D��
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| 1 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��1 mol H2O�����е�ԭ����ΪNA |
| B�����³�ѹ�£�32g O2���е���ԭ����Ϊ2NA |
| C�����³�ѹ�£�11.2L���������ķ�����ΪNA |
| D��1L 0.1mol/L NaCl��Һ��������Na+ΪNA |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com