
A、 |
B、 |
C、 |
D、 |
 ,故A错误;
,故A错误; ,故B正确;
,故B正确;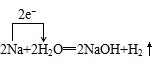 ,故C错误;
,故C错误; ,故D错误.
,故D错误.

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、通入CH4的电极为负极 |
| B、正极发生还原反应 |
| C、此电池工作时溶液中阴离子向正极移动 |
| D、该电池使用一段时间后应补充KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、热的稀硫酸 |
| B、不用稀硫酸,改用98%浓硫酸 |
| C、滴加少量AgNO3溶液 |
| D、不用铁片,改用铁粉 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、实验室用氯化铵和氢氧化钙制氨气:NH4++OH-
| ||||
| B、FeCl3溶液中加入过量的HI溶液:Fe3++2I-=Fe2++I2 | ||||
| C、Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O | ||||
| D、酸化NaNO2溶液:NO2-+H+=HNO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、相对原子质量和质子数 |
| B、次外层电子数和电子层数 |
| C、最外层电子数和次外层电子数 |
| D、电子层数和最外层电子数 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com