
| A£® | Ö»ÓŠ¢ŁÕżČ· | B£® | Ö»ÓŠ¢Ś“ķĪó | C£® | ¢Ł¢Ū¢ÜÕżČ· | D£® | ¢Ł¢Ś¢Ū¢Ü¢ŻČ«“ķ |
·ÖĪö ¢ŁĆ»ÓŠ480mLµÄČŻĮæĘ棬±ŲŠė²ÉÓĆÉŌ“óŅ»µćµÄ500mLµÄČŻĮæĘ棻
¢ŚĶŠÅĢĢģĘ½æɾ«Č·µ½0.1g£»
¢Ūøł¾ŻµĪ¶Ø¹ÜµÄ¾«Č·¶Čæ¼ĀĒ£¬¾«Č·µ½0.01mL£»
¢Ü¹ć·ŗpHŹŌÖ½²āµĆČÜŅŗµÄpHÖµÓ¦ŹĒÕūŹż£»
¢ŻÓĆŅŅ“¼ŗĶÅØH2SO4ÖʱøŅŅĻ©Ź±£¬ŠčŅŖ¼ÓČČÖĮ170”ę£®
½ā“š ½ā£ŗ¢ŁČŻĮæĘæµÄ¹ęøńŗĶĖłÅäÖʵÄČÜŅŗµÄĢå»żĻą·ū£¬Ć»ÓŠ480mLµÄČŻĮæĘ棬±ŲŠė²ÉÓĆÉŌ“óŅ»µćµÄ500mLµÄČŻĮæĘ棬¹Ź¢ŁÕżČ·£»
¢ŚĶŠÅĢĢģĘ½æɾ«Č·µ½0.1g£¬²»ÄÜÓĆĶŠÅĢĢģĘ½³ĘČ”5.85gNaCl£¬¹Ź¢Ś“ķĪó£»
¢ŪµĪ¶Ø¹ÜµÄ¶ĮŹż¾«Č·µ½0.01mL£¬Ėį¼īÖŠŗĶµĪ¶ØŹ±£¬ĻūŗÄ0.1000mol/LµÄŃĪĖį23.0mL“ķĪó£¬Ó¦ĪŖ23.00mL£¬¹Ź¢Ū“ķĪó£»
¢Ü¹ć·ŗpHŹŌÖ½²āµĆČÜŅŗµÄpHÖµÓ¦ŹĒÕūŹż£¬²»æÉÄÜĪŖ7.4£¬¹Ź¢Ü“ķĪó£»
¢ŻÓĆŅŅ“¼ŗĶÅØH2SO4ÖʱøŅŅĻ©Ź±£¬ŠčŅŖŃøĖŁ¼ÓČČÖĮ170”ę£¬Ė®Ō”¼ÓČČ“ļ²»µ½“ĖĪĀ¶Č£¬¹Ź¢Ż“ķĪó£»
¹ŹŃ”A£®
µćĘĄ ±¾Ģāæ¼²é»ÆѧŹµŃé·½°øµÄĘĄ¼Ū£¬Éę¼°ĮæĶ²µÄŹ¹ÓĆ·½·ØŗĶĢģĘ½µÄ¾«Č·¶ČŅŌ¼°µĪ¶Ø¹Ü”¢PHŹŌÖ½µÄ¶ĮŹż£¬ÕĘĪÕ³£ÓĆŅĒĘ÷µÄŹ¹ÓĆ·½·ØŗĶ×¢ŅāŹĀĻīŹĒ½ā“š¹Ų¼ü£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø
ĆūŹ¦µć²¦¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
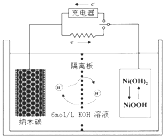 ¾ŻŠĀ»ŖÉē2009Äź5ŌĀ9ČÕµē£¬¹śĪńŌŗ×ÜĄķĪĀ¼Ņ±¦Ö÷³ÖÕŁæŖ¹śĪńŌŗ³£Īń»įŅ飬»įÉĻĶعżĮĖĪŅ¹ś2009Äź½«Ķ¶Čė“óĮæ׏½š·¢Õ¹ŠĀÄÜŌ“Ęū³µ£¬Ö§³Ö½ŚÄÜ”¢»·±£”¢°²Č«µČ¹Ų¼ü¼¼ŹõæŖ·¢£¬ĪŖĪŅ¹śÉē»į¾¼Ćæɳ֊ų·¢Õ¹“ņĻĀĮ¼ŗĆ»ł“”£¬ĪŖ½ńŗóøÄÉĘ»·¾³”¢ĢįÉżĆńÖŚµÄÉś»īÖŹĮæ¾ßÓŠ¼«ĪŖÖŲŅŖµÄŅāŅ壮Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
¾ŻŠĀ»ŖÉē2009Äź5ŌĀ9ČÕµē£¬¹śĪńŌŗ×ÜĄķĪĀ¼Ņ±¦Ö÷³ÖÕŁæŖ¹śĪńŌŗ³£Īń»įŅ飬»įÉĻĶعżĮĖĪŅ¹ś2009Äź½«Ķ¶Čė“óĮæ׏½š·¢Õ¹ŠĀÄÜŌ“Ęū³µ£¬Ö§³Ö½ŚÄÜ”¢»·±£”¢°²Č«µČ¹Ų¼ü¼¼ŹõæŖ·¢£¬ĪŖĪŅ¹śÉē»į¾¼Ćæɳ֊ų·¢Õ¹“ņĻĀĮ¼ŗĆ»ł“”£¬ĪŖ½ńŗóøÄÉĘ»·¾³”¢ĢįÉżĆńÖŚµÄÉś»īÖŹĮæ¾ßÓŠ¼«ĪŖÖŲŅŖµÄŅāŅ壮Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ| ĪļÖŹ | H2 | CO | CH4 |
| ČČÖµ/kJ•g-1 | 143 | 10 | 56 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øŗ¼«·¢ÉśµÄµē¼«·“Ó¦æÉÄÜŹĒ£ŗO2+4e-+2H2OØT4OH - | |
| B£® | Õż¼«·¢ÉśµÄµē¼«·“Ó¦æÉÄÜŹĒ£ŗO2+4e-ØT2O2- | |
| C£® | Õż¼«·“Ó¦Ö÷ŅŖŹĒ£ŗC6H12O6Éś³ÉCO2»ņCO32- | |
| D£® | øŗ¼«·“Ó¦Ö÷ŅŖŹĒ£ŗC6H12O6Éś³É CO2»ņ HCO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £¬NaŌŚŃõĘųÖŠĶźČ«Č¼ÉÕĖłµĆ²śĪļµÄµē×ÓŹ½
£¬NaŌŚŃõĘųÖŠĶźČ«Č¼ÉÕĖłµĆ²śĪļµÄµē×ÓŹ½
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ŌŚ200mLŗ¬Mg2+”¢Al3+”¢NH4+”¢H+”¢Cl-µČĄė×ÓµÄČÜŅŗÖŠ£¬ÖšµĪ¼ÓČė5mol/LµÄĒāŃõ»ÆÄĘČÜŅŗ£¬Ėł¼ÓĒāŃõ»ÆÄĘČÜŅŗµÄĢå»ż£ØmL£©Óė²śÉś³ĮµķµÄĪļÖŹµÄĮæ£Ømol£©¹ŲĻµČēÓŅĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©
ŌŚ200mLŗ¬Mg2+”¢Al3+”¢NH4+”¢H+”¢Cl-µČĄė×ÓµÄČÜŅŗÖŠ£¬ÖšµĪ¼ÓČė5mol/LµÄĒāŃõ»ÆÄĘČÜŅŗ£¬Ėł¼ÓĒāŃõ»ÆÄĘČÜŅŗµÄĢå»ż£ØmL£©Óė²śÉś³ĮµķµÄĪļÖŹµÄĮæ£Ømol£©¹ŲĻµČēÓŅĶ¼ĖłŹ¾£®ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | ŌČÜŅŗÖŠc£ØH+£©=0.1mol/L | B£® | xÓėyµÄ²īÖµĪŖ0.01 mol | ||
| C£® | ŌČÜŅŗÖŠc£ØCl-£©=0.75 mol/L | D£® | ŌČÜŅŗÖŠn£ØMg2+£©£ŗn£ØAl3+£©=5£ŗ1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | »ÆѧĪ£ĻÕĘ·Ī£ŗ¦ČĖĄą½”æµ£¬Ó¦½ūÖ¹Éś²ś | |
| B£® | ĻõĖį¼Ų³ŹÖŠŠŌ£¬ÓėĒā»ÆÄĘŅ»Ęš“¢“ę²»“ęŌŚĪ£ĻÕ | |
| C£® | Ēč»ÆĒā”¢Ēč»ÆÄĘ¾łĪŖ¾ē¶¾£¬ŹÜĒč»ÆÄĘĪŪČ¾µÄĶĮČĄæÉÓĆĖ«ŃõĖ®Ńõ»Æ£¬ĪŖŌöĒ抧¹ūæÉĻČÓĆĮņĖįĖį»Æ | |
| D£® | ÕāŠ©»ÆŃ§Ę·Č¼ÉÕ²śÉśµÄ»šŃę²»ÄÜÓĆĖ®Ö±½ÓĘĖĆš£¬Ö»ÄÜĶعżÓĆɳĶĮø²øĒøō¾ųČ¼ÉÕ»·¾³ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® |  ĻņŹŌ¹ÜÄŚ¼ÓŠæĮ£ | B£® |  ĻņŹŌ¹ÜÄŚµ¹ŅŗĢå | ||
| C£® |  øųŹŌ¹ÜÄŚµÄŅŗĢå¼ÓČČ | D£® |  ÓĆĻš½ŗČūČū×”ŹŌ¹Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½į¹¹Ź¾ŅāĶ¼ £¬æÉŅŌ±ķŹ¾Ņ»ÖÖŌ×Ó£¬Ņ²æÉŅŌ±ķŹ¾Ņ»ÖÖĄė×Ó £¬æÉŅŌ±ķŹ¾Ņ»ÖÖŌ×Ó£¬Ņ²æÉŅŌ±ķŹ¾Ņ»ÖÖĄė×Ó | |
| B£® | ±ČĄżÄ£ŠĶ æÉŅŌ±ķŹ¾¶žŃõ»ÆĢ¼·Ö×Ó£¬Ņ²æÉŅŌ±ķŹ¾¶žĮņ»ÆĢ¼·Ö×Ó·Ö×Ó æÉŅŌ±ķŹ¾¶žŃõ»ÆĢ¼·Ö×Ó£¬Ņ²æÉŅŌ±ķŹ¾¶žĮņ»ÆĢ¼·Ö×Ó·Ö×Ó | |
| C£® | µē×ÓŹ½ æÉŅŌ±ķŹ¾ōĒ»ł£¬Ņ²æÉŅŌ±ķŹ¾ĒāŃõøłĄė×Ó æÉŅŌ±ķŹ¾ōĒ»ł£¬Ņ²æÉŅŌ±ķŹ¾ĒāŃõøłĄė×Ó | |
| D£® | ·Ö×ÓŹ½C2H4O2£ŗæÉŅŌ±ķŹ¾ŅŅĖį£¬Ņ²æÉŅŌ±ķŹ¾¼×Ėį¼×õ„ |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com