
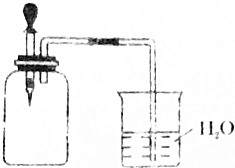
 ��ͼ��ʾ����1molCH4��1molCl2��Ϻ���뼯��ƿ�ڣ����ڹ��������û�����建���ط�Ӧһ��ʱ�䣮
��ͼ��ʾ����1molCH4��1molCl2��Ϻ���뼯��ƿ�ڣ����ڹ��������û�����建���ط�Ӧһ��ʱ�䣮���� ��1�������������ڹ��������·���ȡ����Ӧ����һ�ȼ��顢���ȼ��顢���ȼ��顢���Ȼ�̼���Ȼ��⣻
��2�������������ڹ��������·�Ӧ����һ�ȼ�����Ȼ��⣻
��3����������鷢��ȡ����Ӧ���ɲ�����ֻ���Ȼ����һ�ȼ���Ϊ���壬����ΪҺ�壬����Ȼ���������ˮ�����ʽ��
��4����������ȡ��������ʵ�����Ƚ��̼ԭ���غ����ȡ��������ʵ������ٸ��ݱ�ȡ������ԭ�Ӻ���������֮��Ĺ�ϵʽ�����������������ʵ�����
��� �⣺��1�������������ڹ��������·���ȡ����Ӧ����һ�ȼ��顢���ȼ��顢���ȼ��顢���Ȼ�̼���Ȼ��⣻
�ʴ�Ϊ��һ�ȼ��顢���ȼ��顢���ȼ��顢���Ȼ�̼���Ȼ��⣻
��2���������������ȡ����Ӧ��һ����Ӧ����һ�ȼ�����Ȼ��⣬����ʽΪCH4+Cl2$\stackrel{����}{��}$CH3Cl+HCl���ʴ�Ϊ��CH4+Cl2$\stackrel{����}{��}$CH3Cl+HCl��
��3����������鷢��ȡ����Ӧ���ɲ�����ֻ���Ȼ����һ�ȼ���Ϊ���壬����ΪҺ�壬����Ȼ���������ˮ�����պι��ڵ�ˮ���뼯��ƿ�У��Ȼ�������ˮ��ʹ����ƿ����ѹ��С����������ѹ�����£��ձ��е����뼯��ƿ�У�
�ʴ�Ϊ���ձ��е�ˮ��������ƿ����������鷢��ȡ����Ӧ���ɲ�����ֻ���Ȼ����һ�ȼ���Ϊ���壬����ΪҺ�壬�Ȼ�������ˮ��ʹ����ƿ����ѹ��С����������ѹ�����£��ձ��е����뼯��ƿ�У�
��4��1mol������ȫ����������ȡ����Ӧ����������ͬ���ʵ���������ȡ�������ÿ��ȡ��������ʵ�����0.25mol�������������ȡ����Ӧ�У���ȡ������ԭ�ӵ����ʵ��������������ʵ�����ȣ�
��������0.25molһ�ȼ�����Ҫ����0.25mol������
����0.25mol���ȼ�����Ҫ����0.5mol��
����0.25mol���ȼ�����Ҫ����0.75mol������
����0.25mol���Ȼ�̼��Ҫ����1mol��
�����ܹ��������������ʵ���=0.25mol+0.5mol+0.75mol+1mol=2.5mol��
�ʴ�Ϊ��2.5��
���� ���⿼���˼�������ʣ���ȷ����Ľṹ�����ʼ������ȡ����Ӧ�б�ȡ������ԭ�Ӻ�����֮��Ĺ�ϵ�ǽⱾ��Ĺؼ�����Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
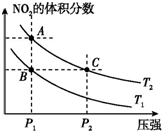
| A�� | ���ֲ�ͬ���¶ȱȽϣ�T1��T2 | |
| B�� | A��C����ķ�Ӧ���ʣ�A��C | |
| C�� | B��C����������ƽ����Է���������B��C | |
| D�� | ��״̬B��״̬A�������ü��ȵķ���ʵ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Al�ܷų�H2����Һ�У�ClO-��HCO${\;}_{3}^{-}$��SO${\;}_{4}^{2-}$��NH${\;}_{4}^{+}$ | |
| B�� | pH=2����Һ�У�Fe2+��Na+��Mg2+��NO${\;}_{3}^{-}$ | |
| C�� | ��ʹKSCN��Һ������Һ�У�Na+��I-��NO${\;}_{3}^{-}$��HCO${\;}_{3}^{-}$ | |
| D�� | ��ˮ�������c��OH-��=1.0��10-13mol•L-1����Һ�У�Na+��Ba2+��Cl-��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
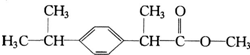 ij��ҩ����Ҫ�ɷ�X�ķ��ӽṹ��ͼ�������л���X��˵���д�����ǣ�������
ij��ҩ����Ҫ�ɷ�X�ķ��ӽṹ��ͼ�������л���X��˵���д�����ǣ�������| A�� | �٢� | B�� | �ڢ� | C�� | �ڢ� | D�� | �٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
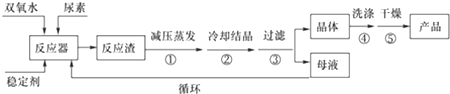
| ����ʽ | ��� | �ȷֽ��¶� | �۵� | �ܽ��� |
| CO��NH2��2•H2O2 | ��ɫ���� | 45�� | 75-85�� | ������ˮ���л��ܼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | Ǧ���ص�A��Ϊ�������缫����ΪPbO2 | |
| B�� | Ǧ���طŵ�ʱ������������ | |
| C�� | �õ��ص�������ӦΪ��2 NO3-+6H2O+10e-�TN2��+2OH- | |
| D�� | ����·������2mol���ӣ�����������Һ��������32g�������������Һ�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com