
钯的化合物PdCl2通过化学反应可用来检测有毒气体CO,该反应的反应物与生成物有CO、Pd、H2O、HCl、PdC12和一种未知物质X。下列说法错误的是( )
A.未知物质X为CO2,属于氧化产物 B.每转移1mol e- 时,生成2 molX
C.反应中PdCl2作氧化剂,被还原 D.还原性:CO>Pd
科目:高中化学 来源:2016-2017学年河北省卓越联盟高一上第一次月考化学试卷(解析版) 题型:选择题
在标准状况下,将1.40g氮气、1.60g氧气和4.00g氩气充分混合,则该混合气体的体积为( )
A.2.24L B.3.36L C.4.48L D.无法计算
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省卓越联盟高二上第一次月考化学试卷(解析版) 题型:选择题
已知2H2(g)+O2(g)=2H2O(g)ΔH1;2H2(g)+O2(g)=2H2O(l)ΔH2。则下列关于ΔH1与ΔH2大小比较中正确的是( )
A.ΔH1 > ΔH2 B.ΔH1 < ΔH2 C.ΔH1 = ΔH2 D.无法确定
查看答案和解析>>
科目:高中化学 来源:2016-2017学年甘肃省高一上10月月考化学试卷(解析版) 题型:选择题
实验室中需要配制2 mol/L的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )。
A. 950 mL 111.2 g B. 500 mL 117 g
C. 1 000 mL 117 g D. 任意规格 111.2 g
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第一次阶段考化学试卷(解析版) 题型:实验题
纯净的过氧化钙(CaO2)是白色的结晶粉末,难溶于水,不溶于乙醇、乙醚,常温下较为稳定,是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。在实验室可用钙盐制取CaO2•8H2O,再经脱水制得CaO2。CaO2•8H2O在0℃时稳定,在室温时经过几天就分解,加热至130℃时逐渐变为无水CaO2。其制备过程如下:

回答下列问题:
(1)用上述方法制取CaO2•8H2O的化学方程式是 。为了控制沉淀温度为0℃左右,在实验室宜采取的方法是 。
(2)该制法的副产品为 (填化学式),为了提高副产品的产率,结晶前要将溶液的pH调整到合适范围,可加入的试剂是 。
(3)为了检验“水洗”是否合格,可取少量洗涤液于试管中,再滴加 。
(4)测定产品中CaO2的含量的实验步骤是:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2mol/L的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:用浓度为c mol/L的Na2S2O3溶液进行滴定,消耗Na2S2O3溶液V mL。
(已知:I2+2S2O32-=2I-+S4O62-)
①第三步中滴定终点的现象是 ;
②CaO2的质量分数为 (用字母表示)。
(5)已知CaO2在350℃迅速分解生成CaO和O2。某实验小组设计下图装置测定产品中CaO2含量(夹持装置省略)。

①若所取产品质量是m g,测得气体体积为V mL(已换算成标准状况),则产品中CaO2的质量分数为 (用字母表示)。
②CaO2的含量也可用重量法测定,需要测定的物理量有 。
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次月考化学试卷(解析版) 题型:填空题
[化学——选修2:化学与技术]碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医药卫生等工业领域。铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如下工艺流程得到粗碲。
(1)“加压硫酸浸出”过程中会发生以下化学反应:Cu2Te+2O2=2CuO+TeO2 ;TeO2+H2SO4=TeOSO4+H2O
①Ag2Te也能与O2发生类似Cu2Te的反应,化学方程式为____________。
②工业上给原料气加压的方法是________。
(2)操作Ⅰ是________。
(3)“含碲浸出液”的溶质成分除了TeOSO4外,主要是____________(填化学式)。
(4)“电 解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初始阶段阴极的电极反应式是________。
解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初始阶段阴极的电极反应式是________。
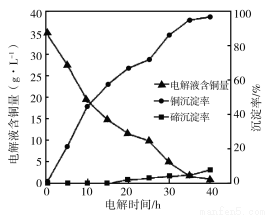
(5)向“含碲硫酸铜母液”通入SO2并加入NaCl反应一段时间后,Te(IV)浓度从6.72 g·L-1下降到0.10 g·L-1,Cu2+浓度从7.78 g·L-1下降到1.10 g·L-1。
①TeOSO4生成Te的化学方程式为________。
②研究表明,KI可与NaCl起相同作用,从工业生产的角度出发选择NaCl最主要的原因是________。
③计算可得Cu2+的还原率为85.9%,Te(IV)的还原率为________。
查看答案和解析>>
科目:高中化学 来源:2017届广东省高三上第二次月考化学试卷(解析版) 题型:选择题
甲、乙、丙三种元素均位于第三周期,其原子序数逐渐增大,甲的最高价氧化物对应的水化物是强碱,乙是地壳中含量最多的金属元素,丙是本周期中原子半径最小的元素。下列说法不正确的是( )
A. 甲是第IA元素,丙是第VIIA元素 B. 甲、丙形成的化合物是离子化合物
C. 乙的最高价氧化物是两性氧化物 D. 丙是元素周期表中非金属性最强的元素
查看答案和解析>>
科目:高中化学 来源:2017届福建省四地六校高三上第一次月考化学试卷(解析版) 题型:选择题
下列离子方程式书写正确的是( )
A.氧化亚铁溶于稀硝酸:FeO + 2H+ == Fe2+ + H2O
B.往CaCl2溶液中通入少量的CO2: Ca2++CO2+H2O=CaCO3↓+2H+
C.碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3- + OH-=CO32-+ H2O
D.向澄清石灰水中滴加少量的NaHCO3溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上10月月考化学试卷(解析版) 题型:选择题
在密闭的容器中的一定量混合气体发生反应,xA(g)+yB(g)  zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容器扩大到原来的两倍,在达平衡时,测得A的浓度降低为0.5 mol/L.下列有关判断正确的是
zC(g),平衡时测得A的浓度为0.80mol/L,保持温度不变,将容器的容器扩大到原来的两倍,在达平衡时,测得A的浓度降低为0.5 mol/L.下列有关判断正确的是
A.x+y<z B.平衡向正反应方向移动 C.B的转化率升高 D.C的体积分数下降
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com