
 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案科目:高中化学 来源:不详 题型:单选题
| A.晶体熔点由低到高:CF4< CCl4< CBr4< CI4 |
| B.硬度由大到小:金刚石 > 碳化硅 > 晶体硅 |
| C.熔点由高到低:Na > Mg > Al |
| D.晶体的熔点高低规律一般有:原子晶体 > 离子晶体 > 分子晶体 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| A.分子晶体 | B.原子晶体 | C.离子晶体 | D.金属晶体 E.混合晶体 |
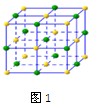
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素 | 相关信息 |
| T | T原子所处的周期数、族序数分别与其原子序数相等 |
| X | X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | Z的基态原子价电子排布为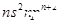 |
| Q | 在该元素所在周期中,Q的基态原子的第一电离能最小 |
| R | 3p能级上有1个电子 |
| W | W的一种核素的质量数为65,中子数为36 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A. | B. |
| C. | D.NA·a3·ρ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有些物质是由分子直接构成的,如二氧化碳、二氧化硅;有些物质是由原子直接构成,如金刚石、晶体硅;有些是由离子直接构成的,如氯化铵 |
| B.分子是保持物质性质的一种微粒,且是化学变化中的最小微粒 |
| C.在水溶液中能电离出自由移动离子的晶体不一定是离子晶体 |
| D.使晶体中化学键断裂的变化一定是化学变化 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③⑥ | B.①②④ | C.②④⑥ | D.③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
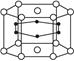
| A.MgB | B.MgB2 | C.Mg2B | D.Mg3B2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com