
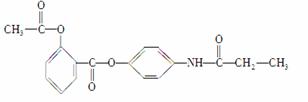
某有机化合物A的结构简式如下:
(1)A的分子式是__________________。
(2)A在NaOH水溶液中充分加热后,再加入过量的盐酸酸化后,可得到B、C、D和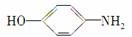 四种有机物,且相对分子质量大小关系为B>C>D。则B、C、D的结构简式分别是:B____________________;C________________;D__________________。
四种有机物,且相对分子质量大小关系为B>C>D。则B、C、D的结构简式分别是:B____________________;C________________;D__________________。
(3)下列物质中,不能与B发生化学反应的是(填序号)________。
①浓H2SO4和浓HNO3的混合液 ②CH3CH2OH(酸催化) ③CH3CH2CH2CH3 ④Na ⑤浓溴水
(4)在B的同分异构体中,属于1,3,5三取代苯的化合物的结构简式为
________________________________________________________________________。
(5)写出B与碳酸氢钠反应的化学方程式:
________________________________________________________________________。
科目:高中化学 来源: 题型:
灰锡(以粉末状存在)和白锡是锡的两种同素异形体。已知:
①Sn(s,白)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH1
②Sn(s,灰)+2HCl(aq)===SnCl2(aq)+H2(g) ΔH2
③Sn(s,灰)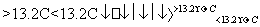 Sn(s,白) ΔH3=+2.1 kJ·mol-1
Sn(s,白) ΔH3=+2.1 kJ·mol-1
下列说法正确的是( )
A.ΔH1>ΔH2
B.锡在常温下以灰锡状态存在
C.灰锡转化为白锡的反应是放热反应
D.锡制器皿长期处在低于13.2 °C的环境下,会自行毁坏
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于金属键的叙述中,不正确的是 ( )。
A.金属键是金属阳离子和自由电子这两种带异性电荷的微粒间的强烈相互
作用,其实质与离子键类似,也是一种电性作用
B.金属键可以看作是许多原子共用许多电子所形成的强烈的相互作用,所
以与共价键类似,也有方向性和饱和性
C.金属键是带异性电荷的金属阳离子和自由电子间的相互作用,故金属键
无饱和性和方向性
D.构成金属键的自由电子在整个金属内部的三维空间中做自由运动
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质既不是同系物又不是同分异构体的是( )
A.软脂酸甘油酯和硬脂酸甘油酯 B.甲酸甲酯和乙酸
C.对甲基苯酚和苯甲醇 D.油酸甘油酯和乙酸乙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
葡萄糖的分子式为C6H12O6,通过缩合反应把10个葡萄糖分子连接起来所形成的链状化合物的分子式为( )
A.C60H120O60 B.C60H100O52
C.C60H102O51 D.C60H112O51
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.硬脂酸和软脂酸都属于酸,一个是饱和酸,一个是不饱和酸
B.植物油不能使溴的四氯化碳溶液褪色
C.柴油可以在碱性条件下水解
D.可通过反应后的溶液不分层,判断油脂的皂化反应基本完成
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下铁可以和CO2发生反应:Fe(s)+CO2(g)FeO(s)+CO(g) ΔH>0,1 100 ℃时,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2和CO的浓度与时间的关系如图所示。
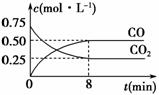
(1)该反应的平衡常数表达式K=________。
(2)下列措施中能使平衡常数K增大的是________(填序号)
A.升高温度 B.增大压强
C.充入一定量CO D.降低温度
(3)8 min内,CO的平均反应速率v(CO)=________mol·L-1·min-1。
(4)1 100 ℃时,2 L的密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下:
| 容器 | 甲 | 乙 |
| 反应物投入量 | 3 mol Fe、2 mol CO2 | 4 mol FeO、3 mol CO |
| CO的浓度(mol·L-1) | c1 | c2 |
| CO2的体积分数 | φ1 | φ2 |
| 体系压强(Pa) | p1 | p2 |
| 气态反应物的转化率 | α1 | α2 |
①下列说法正确的是________。
A.2c1=3c2 B.φ1=φ2
C.p1<p2 D.α1=α2
②求c1=________、φ1=________、α2=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
能源危机当前是一个全球性问题,开源节流是应对能源危机的重要举措。
(1)下列做法有助于“开源节流”的是________(填序号)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气,以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、减少使用煤、石油等化石燃料
d.减少资源消耗,注重资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。
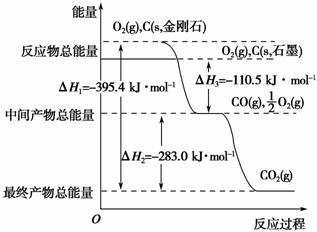
①在通常状况下,金刚石和石墨相比较,________(填“金刚石”或“石墨”)更稳定,石墨的燃烧热为________。
②12 g石墨在一定量的空气中燃烧,生成气体36 g,该过程放出的热量为________。
(3)已知:N2、O2分子中化学键的键能分别是946 kJ·mol-1、497 kJ·mol-1。
N2(g)+O2(g)===2NO(g) ΔH=+180.0 kJ·mol-1
NO分子中化学键的键能为________ kJ·mol-1。
(4)综合上述有关信息,请写出用CO除去NO的热化学方程式:________________________________________________________________
_____________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com