
 一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯).反应原理:
一硝基甲苯是一种重要的工业原料,某化学学习小组设计如图所示装置制备一硝基甲苯(包括对硝基甲苯和邻硝基甲苯).反应原理: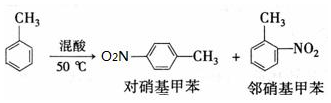
 .
.
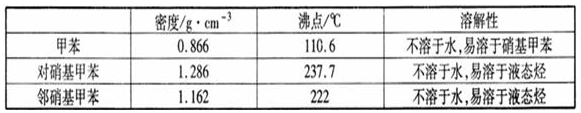
分析 制备一硝基甲苯:分别量取浓硫酸和浓硝酸,将浓硝酸倒入烧杯中,浓硫酸沿着烧杯内壁缓缓注入,并不断搅拌,配制混合溶液(即混酸),因反应液体沸点较低,加热时容易发生暴沸,所以在三颈瓶中加入沸石,再向三颈瓶中加入混酸,并不断搅拌,控制温度50℃,水浴(水的沸点100℃)目的能均匀加热,且便于控制反应速率,温度约为50℃,反应大约10min,三颈瓶底有大量淡黄色油状液体出现,分离出一硝基甲苯,经提纯最终得到纯净的一硝基甲苯,制得纯净的一硝基甲苯共15g,
(1)如果温度过高,会发生副反应生成二硝基甲苯、三硝基甲苯等副产品;
(2)浓硫酸的密度大于硝酸,浓硝酸中有水,浓硫酸溶于水会放热,据此确定配制混酸的方法;
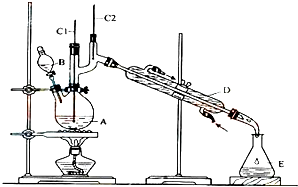
(3)根据装置图可知,仪器A是球形冷凝管,用于冷凝回流,水流方向为逆流;
(4)甲苯与混酸发生取代反应生成对硝基甲苯和水;
(5)分离两种不相溶的液体用分液;分离两种沸点的不同液体,采用蒸馏的方法,所以操作2为蒸馏,据此判断需要的仪器;
(6)根据产率=$\frac{实际量}{理论量}$×100%计算.
解答 解:(1)本实验的关键是控制温度在30℃左右,如果温度过高,会发生副反应生成二硝基甲苯、三硝基甲苯等副产品,故答案为:二硝基甲苯、三硝基甲苯;
(2)浓硫酸的密度大于硝酸,浓硝酸中有水,浓硫酸溶于水会放热,所以配制混合酸的方法是:量取浓硝酸倒入烧杯中,再量取浓硫酸沿烧杯内壁缓缓注入烧杯并不断用玻璃棒搅拌,
故答案为:量取一定量浓硝酸倒入烧杯中,再量取浓硫酸沿烧杯内壁缓缓注入烧杯,并用玻璃棒不断搅拌;
(3)根据装置图可知,仪器A是球形冷凝管,用于冷凝回流,充分利用原料,提高生成物的产量,水流方向为逆流,进水口为a,
故答案为:球形冷凝管;a;
(4)甲苯与混酸加热发生取代反应,生成对硝基甲苯和水,反应的化学方程式为 ,
,
故答案为: ;
;
(5)因为分离得到的是无机和有机两种液体,而有机物和无机物是不相溶的,因此操作1是分液;分离两种沸点的不同液体,采用蒸馏的方法,所以操作2为蒸馏,经测定,产品2的核磁共振氢谱中有5个峰,说明分子中含有5个不同位置的氢原子,有机物名称为邻硝基甲苯,
故答案为:蒸馏;邻硝基甲苯;
(6)在三颈烧瓶里装15mL甲苯(密度为0.866g•cm-3)甲苯质量=0.866g•cm-3 ×15mL=12.99g;根椐方程式,1摩尔的甲苯可以得到1摩尔的对硝基甲苯与1摩尔的邻硝基甲苯,则92g的甲苯可以得到137g的对硝基苯和137g的邻硝基苯.那么12.99g的甲苯就能得到的一硝基苯的质量就是:$\frac{12.99g×137}{92}$=19.34g,所以一硝基苯的产量就应该这样来进行计算:$\frac{15g}{19.34g}$×100%=77.5%,
故答案为:77.5%.
点评 本题主要考查一硝基甲苯的制备,涉及实验流程、产率的计算等知识,题目难度中等,熟悉流程的意义与目的是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | SO2可用于杀菌、消毒 | B. | HF可用于雕刻玻璃 | ||
| C. | NH3可用于制硝酸 | D. | SiO2可用于制太阳能电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某温度时,在容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析:
某温度时,在容积为2L的密闭容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示,由图中数据分析:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如图装置合成正丁醛.发生的反应如下:| 沸点/℃ | 密度/(g•cm-3) | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| v正 | v逆 | 平衡常数K | 转化率α |
| 增大 | 增大 | 减小 | 减小 |
| [CO2]/mol•L-1 | [H2]/mol•L-1 | [CH4]/mol•L-1 | [H2O]/mol•L-1 | |
| 平衡Ⅰ | a | b | c | d |
| 平衡Ⅱ | m | n | x | y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 减少 | B. | 增大 | ||
| C. | 不变 | D. | 无法判断变化情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 潮湿的氯气通过盛有浓H2SO4的洗气瓶 | |
| B. | 硫化氢通入浓H2SO4中 | |
| C. | 浓H2SO4滴入萤石中,加热 | |
| D. | 加入少量H2SO4使乙酸乙酯水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com