
| A. | 化合物电离时,生成的阴离子是氢氧根离子的是碱 | |
| B. | 某化合物的熔融状态能导电,该化合物中一定有离子键 | |
| C. | 某化合物的水溶液能导电,该化合物一定是电解质 | |
| D. | 某纯净物在常温下为气体,则组成该物质的微粒一定含有共价键 |
分析 A、电离时生成的阴离子全部都是氢氧根离子的化合物是碱;
B、离子化合物在熔融状态下会导电,含有离子键的化合物称为离子化合物;
C、水溶液或是熔融状态下导电的化合物称为电解质;
D、稀有气体为单原子分子,不存在化学键.
解答 解:A、化合物电离时生成的阴离子全部都是氢氧根离子的化合物是碱,故A错误;
B.熔融状态能导电的化合物,说明存在自由移动的离子,离子之间靠离子键结合,故B正确;
C、要看是否自身电离出离子;氨气的水溶液能导电,氨气不是电解质,而氨气溶于水和水结合的一水合氨为电解质,故C错误;
D.稀有气体为单原子分子,不存在化学键,故D错误;
故选B.
点评 本题考查了一些基本概念,难度较小.注意一些特例,如稀有气体中不存在化学键等.


科目:高中化学 来源: 题型:选择题
| A. | 100 mL 1mol/L NaCl溶液 | B. | 75mL 1 mol/L MgCl2溶液 | ||
| C. | 150 mL 3mol/L KCl溶液 | D. | 25 mL 2 mol/L AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 正反应放热 | B. | 加水平衡不移动 | ||
| C. | 加入K2SO4固体,平衡向左移动 | D. | 加入K2SO4溶液,平衡向左移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都属于碱性氧化物 | B. | 溶于水后,所得水溶液的成分相同 | ||
| C. | 都能和水发生化合反应 | D. | 都可和二氧化碳反应生成不同的盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X为液态,Z为气态 | B. | X为固态,Z为气态 | C. | X为气态,Z为气态 | D. | 无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O、Na2O2都能与水发生都是碱性氧化物 | |
| B. | Na2O、Na2O2均能与水发生化合反应,生成O2 | |
| C. | Na、Na2O、Na2O2溶于水后形成的溶液其溶质相同 | |
| D. | Na着火可用泡沫灭火器灭火 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 颜色、状态、属于碱性氧化物 | |
| B. | 与盐酸反应所观察到现象 | |
| C. | 长期置放在空气中的最终产物 | |
| D. | 与水反应后滴加酚酞所观察到的现象 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

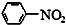 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$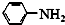 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$

 ;
; ;该反应的目的是保护在硝化过程中醇羟基不被氧化;
;该反应的目的是保护在硝化过程中醇羟基不被氧化; .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
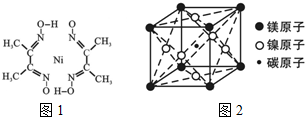 金属镍及其化合物在合金材料以及催化剂等方面应用广泛.根据要求回答下列问题.
金属镍及其化合物在合金材料以及催化剂等方面应用广泛.根据要求回答下列问题. )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com