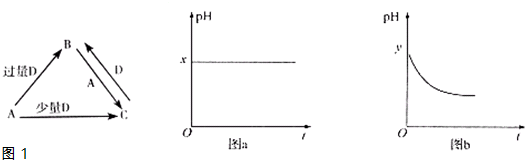
(2014?滨州一模)A、B、C、D均为中学化学中常见的单质或化合物,它们之间的关系如图1所示(部分产物已略去).
(1)若A为金属单质,D是某强酸的稀溶液,则反应B+A→C的离子方程式为
2Fe3++Fe=3Fe2+
2Fe3++Fe=3Fe2+
.
(2)若A、B为盐,D为强碱,A的水溶液显酸性,则反应 A+D→B的离子方程式为
Al3++4OH-=[Al(OH)4]-
Al3++4OH-=[Al(OH)4]-
.
(3)若A为强碱,D为气态酸性氧化物.常温时,将B的水溶液露置于空气中,其pH随时间t变化可能如图a或图b所示(不考虑D的溶解和水的挥发).
①若图a符合事实,则D为
CO2
CO2
(填化学式),此时图a中x
>
>
7(填“>”“<”或“=”)
②若图b符合事实,且图b中y<7,B的焰色反应为黄色,则B溶液中各离子浓度由大到小的顺序是
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
c(Na+)>c(HSO3-)>c(H+)>c(SO32-)>c(OH-)
.



