
(15分)氢化钙固体是登山运动员野外常用的能源提供剂。某化学兴趣小组拟选用如下装置制备氢化钙。已知:氢化钙在一定条件下与氧气反应生成的产物不只一种。

请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为______________(填仪器接口的字母编号)。
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗
活塞;______________(请按正确的顺序填入下列步骤的标号)。
A.加热反应一段时间 B.收集气体并检验其纯度
C.关闭分液漏斗活塞 D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色。该同学据此判断,上述实验确有CaH2生成。
① 写出CaH2与水反应的化学方程式___________________________;
② 该同学的判断是否准确,原因是______________________________。
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象_____。
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是____________________。
(1)i→e,f→d,c→j(或k),k(或j)→a(2分) (2)BADC(2分)
(3)①CaH2 + 2H2O=Ca(OH)2+2H2↑ (3分)
②不准确 金属钙与水反应也有类似现象(2分)
(4)取适量氢化钙,在加热条件下与干燥的氧气反应,将反应的气体产物通过装有无水硫酸铜的干燥管,观察到白色变为蓝色;取钙做类似实验,观察不到白色变蓝色 (4分)
(5)氢化钙是固体,携带方便 (2分)
【解析】
试题分析:(1)钙属于极活泼的金属,极易与水反应生成氢氧化钙和氢气,而制备的氢气中会混有水蒸气和氯化氢,所以在与钙化合之前需要除杂和干燥,分别选用试剂是氢氧化钠和浓硫酸;同时为防止空气中水蒸气进入,最后还需要连接干燥管,所以正确的顺序为:i→e,f→d,c→j(或k),k(或j)→a;
(2)由于多余的氢气需要燃烧反应掉,所以应该先收集一部分气体并检验其纯度,反应结束后还需要使氢化钙在氢气的氛围中冷却,所以应该最后关闭分液漏斗活塞,因此正确的顺序为BADC;
(3)①CaH2与水反应能产生Ca(OH)2和H2,反应方程式为:CaH2+2H2O=Ca(OH)2+2H2↑;
②CaH2和Ca与水反应都能产生Ca(OH)2和H2,反应方程式分别为:CaH2+2H2O=Ca(OH)2+2H2↑和Ca+2H2O=Ca(OH)2+H2↑,因此不能根据反应后溶液呈碱性判断是否含有CaH2;
(4)CaH2可以和氧气在加热条件下反应生成水,可用无水硫酸铜检验,现象是白色变为蓝色,即操作为:取适量氢化钙,在加热条件下与干燥的氧气反应,将反应的气体产物通过装有无水硫酸铜的干燥管,观察到白色变为蓝色;取钙做类似实验,观察不到白色变蓝色;
(5)作为能源,氢化钙明显比氢气更易携带,使用也较方便。
考点:考查考查元素化合物知识,涉及到物质的性质和制备实验


 星级口算天天练系列答案
星级口算天天练系列答案科目:高中化学 来源:2013-2014福建省高三高考模拟理综化学试卷(解析版) 题型:选择题
制备乙酸乙酯的绿色合成路线之一为:

下列说法不正确的是
A.M的分子式为C6H12O6 B.N的结构简式为CH3COOH
C.④的反应类型属于取代反应 D.淀粉与纤维素互为同分异构体
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:填空题
为了研究碳酸钙与稀盐酸反应的反应速率,一位同学通过实验测定反应 中生成的CO2气体体积随反应时间变化的情况,绘制曲线。请分析讨论以下问题。
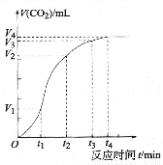
(1)碳酸钙与稀盐酸的反应是放热反应,这是由于反应物的总能量______(填“大于”或“小于”)生成物的总能量。
(2)在0~t1、t1~t2、t2~t3、t3~t4各相同的时间段里, 收集到气体最多的是_____时间段。反应速率最大的是__________时间段,反应速率最小的是__________时间段。
(3)t1~t2时间段里影响反应速率的主要外界因素是 、t2~t3时间段里影响反应速率的主要外界因素是 (填“温度”或“浓度” 或“压强” 或“催化剂”)(提醒:多填不得分)
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
下列物质性质比较正确的是( )
A.热稳定性:HCl>H2S>H2O B.离子半径:Na+>Cl->F-
C.碱性:NaOH>Mg(OH)2>Al(OH)3 D.熔点:金刚石>干冰>食盐
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省福州八县第二学期期中考试高一化学试卷(解析版) 题型:选择题
下列有关离子键、共价键的叙述中正确的是( )
A.离子化合物中只存在离子键,没有共价键
B.构成单质分子的粒子中一定含有共价键
C.共价化合物分子中一定不存在离子键
D.仅由非金属元素组成的化合物中一定不含离子键
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高三5月校质检理综化学试卷(解析版) 题型:选择题
下列实验能达到目的的是( )
|
|
|
|
A. 检验SO2具有漂白性 | B.配制0.1 mol?L-1NaOH溶液时定容 | C.分离出碘水中的碘 | D.配制一定浓度硫酸溶液 |
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省漳州市八校高三第四次联考理综化学试卷(解析版) 题型:实验题
(15分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:
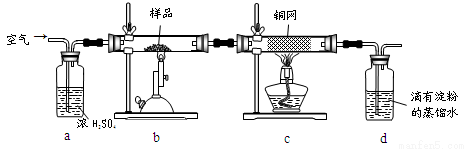
现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的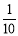 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
(1)称量样品所用的仪器为_____(填“托盘天平”或“电子天平”),将样品研细后再反应,其目的是_______ 。
(2)装置a和c的作用分别是____和____(填标号)。
A.除去SO2气体 B.除去空气中的水蒸气 C.有利于气体混合
D.有利于观察空气流速 E.除去反应后多余的氧气
(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)通过计算可知,该黄铜矿的纯度为________。
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____(填序号)。
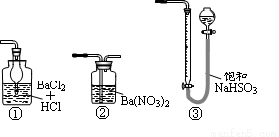
(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有_____________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省高二下学期期末考试化学试卷(解析版) 题型:选择题
常温下,将VL0.10mol·L-1盐酸和VL0.06mol·L-1Ba(OH)2溶液混合后,该混合液的pH为(设混合后总体积为2VL)
A.1.7 B.12.3 C.12 D.2
查看答案和解析>>
科目:高中化学 来源:2013-2014福建省四地六校高三高考模拟试理综化学试卷(解析版) 题型:选择题
下列说法不正确的是( )
A. 服用铬含量超标的药用胶囊会对人对健康造成危害
B. 食用一定量的油脂能促进人体对某些维生素的吸收
C.CH4和Cl2在光照条件下反应的产物最多可能有四种
D.无论乙烯的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com