
| A | B | C | D |
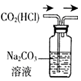 | 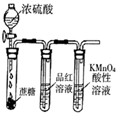 | 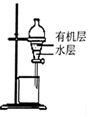 | 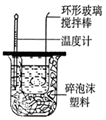 |
| 除去CO2中含有的少量HCl气体 | 说明浓H2SO4具有脱水性,强氧化性,SO2具有漂白性、还原性 | 将有机层从分液漏斗下口放出 | 用于中和反应反应热的测定 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.二者都与碳酸钠反应;
B.浓硫酸可使蔗糖变黑,碳与浓硫酸发生氧化还原反应;
C.有机物在上层,应从上口倒出;
D.温度计位置错误.
解答 解:A.二者都与碳酸钠反应,不能用于除杂,应用碳酸氢钠溶液,故A错误;
B.浓硫酸使蔗糖变黑,体现脱水性,与C反应生成二氧化硫,体现其强氧化性,图中品红褪色,说明二氧化硫具有漂白性,高锰酸钾溶液褪色,发生氧化还原反应,说明二氧化硫具有还原性,所以图中装置能说明浓H2SO4具有脱水性、强氧化性,SO2具有漂白性、还原性,故B正确;
C.分液时,上层液体从上口倒出,下层液体凑从下端流出,有机物在上层,应从上口倒出,故C错误;
D.温度计用于测量反应液的温度,应位于小烧杯中,故D错误.
故选B.
点评 本题考查化学实验方案的评价,为高考常见题型,侧重考查学生的分析能力和实验能力,题目涉及混合物的分离、物质的性质、中和热的测定,注意把握物质的性质以及实验的严密性和可行性的评价,题目难度中等.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:选择题
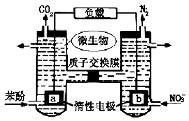
| A. | a电极为正极 | |
| B. | H+由右室通过质子交换膜进入左室 | |
| C. | a电极反应式为:C6H5OH-28e-+11H2O═6CO2↑+28H+ | |
| D. | 当b电极上产生lmol N2时,溶液中将有l0mol e-通过 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Br>Ga>Cl>Al | |
| B. | 碱性:Ga(OH)3>Al(OH)3 酸性:HClO4>HBrO4 | |
| C. | 7935Br与8135Br得电子能力不同 | |
| D. | 与镓同周期且相邻的主族元素,其原子序数为30或32 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学性质 | 实际应用 | |
| A | 小苏打受热易分解 | 焙制糕点 |
| B | 蛋白质受热变性 | 高温杀死流感病毒 |
| C | SO2具有漂白性 | 漂白滋补品银耳等食品 |
| D | Al(OH)3分解吸收大量热量并有水生成 | 阻燃剂 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 羰基硫是电解质 | B. | 羰基硫分子的电子式为: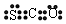 | ||
| C. | C、O、S三个原子中半径最小的是C | D. | 羰基硫分子为非极性分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(H2)=0.05mol/(L•min) | B. | v(N2)=0.03mol/(L•min) | ||
| C. | v(NH3)=0.17g/(L•min) | D. | v(NH3)=0.02mol/(L•min) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢氧化物呈两性 | B. | 单质与水反应放出氢气 | ||
| C. | 在化合物中呈+2价 | D. | 单质的还原性比镁强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com