
【题目】下列做法正确的是( )
A. 将浓硝酸保存在无色玻璃瓶中 B. 金属钠和钾保存在煤油中
C. Na2CO3可以保存在玻璃塞的玻璃瓶中 D. NaOH固体放在滤纸上称量
科目:高中化学 来源: 题型:
【题目】对于化学反应3W(g)+2X(g)=4Y(g)+3Z(g),下列反应速率关系中,正确的是
A.υ(W)=3υ(Z)
B. 3υ(X)=2υ(Z)
C.υ(X)= 2υ(Y)
D. 3υ(W)=2υ(X)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】 某校学生用化学知识解决生活中的问题,下列家庭小实验中不合理的是( )
A.用食醋除去暖水瓶中的薄层水垢
B.用米汤检验含碘盐中的碘酸钾(KIO3)
C.用食用碱(Na2CO3)溶液洗涤餐具上的油污
D.用灼烧并闻气味的方法区别纯棉织物和纯毛织物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了说明稀硝酸与铜反应产生无色的一氧化氮气体,某同学设计了如图所示的实验装置。实验时,将分液漏斗的活塞打开,从U形管的长管口B注入稀硝酸,一直到U形管的短管口A单孔塞下沿且液面不再留有气泡为止。关闭活塞,并用酒精灯在U形管短管下微热。当铜丝上有气泡产生时,立即撤去酒精灯。试回答:

(1)反应一段时间后,除了可以观察到铜丝逐渐溶解,有气泡产生,还会出现的现象有________。
(2)反应结束后,若将活塞缓缓打开,分液漏斗内有何现象______________。
(3)写出生成一氧化氮的离子方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:

(1)四种元素原子半径由大到小的顺序是(写元素符号)_________________________。
(2)元素Y与氢元素形成的一种离子YH4+,写出该微粒的电子式________(用元素符号表示)。
(3)T元素的简单阴离子的结构示意图是______________________,
(4)证明该粒子的还原性比Z-强的离子方程式是____________________.
(5)元素Z的单质与氢氧化钠溶液反应的化学方程式为_______________________ 。
(6)将9g单质X在足量氧气中燃烧,所得气体通入1L 1mol·L-1NaOH溶液中,完全吸收后,将溶液在减压低温条件下蒸干,得到不含结晶水的固体质量为____________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)已知磷酸(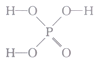 )分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。
)分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。

(2)H3PO2具有较强的还原性,可以通过电解的方法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为_________。
②II 膜为___________(填“阴离子交换膜”或“阳离子交换膜”)。
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的交换膜,从而合并阳极室与产品室,其缺点是产品中混有______杂质。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化碳是一种宝贵的碳氧资源。以CO2和NH3为原料合成尿素是固定和利用CO2的成功范例。在尿素合成塔中的主要反应可表示如下:
反应Ⅰ:2NH3(g)+CO2(g)![]() NH2CO2NH4(s) △H1=a kJ·mol-1
NH2CO2NH4(s) △H1=a kJ·mol-1
反应Ⅱ:NH2CO2NH4(s)![]() CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
CO(NH2)2(s)+H2O(g) △H2=+72.49kJ·mol-1
总反应Ⅲ:2NH3(g)+CO2(g)![]() CO(NH2)2(s)+H2O(g) △H3=-86.98kJ·mol-1
CO(NH2)2(s)+H2O(g) △H3=-86.98kJ·mol-1
请回答下列问题:
(1)反应Ⅰ的△H1= (用具体数据表示)。
(2)反应Ⅱ的△S (填>或<)0,一般在 情况下有利于该反应的进行。
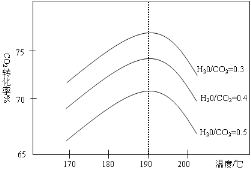
(3)反应Ⅲ中影响CO2平衡转化率的因素很多,下图1为某特定条件下,不同水碳比n(H2O)/n(CO2)和温度影响CO2平衡转化率变化的趋势曲线。
①其他条件相同时,为提高CO2的平衡转化率,生产中可以采取的措施是 (填提高或降低)水碳比。
②当温度高于190℃后,CO2平衡转化率出现如图所示的变化趋势,其原因是 。
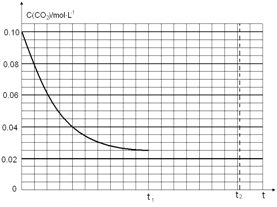
(4)某研究小组为探究反应Ⅰ中影响c(CO2)的因素,在恒温下将0.4molNH3和0.2molCO2放入容积为2L的密闭容器中,t1时达到平衡过程中c(CO2)随时间t变化趋势曲线如上图所示。若其他条件不变,t1时将容器体积压缩到1L,请画出t1后c(CO2)随时间t变化趋势曲线(t2达到新的平衡)。
(5)尿素在土壤中会发生反应CO(NH2)2+2H2O![]() (NH4)2CO3。下列物质中与尿素有类似性质的是
(NH4)2CO3。下列物质中与尿素有类似性质的是
A.NH2COONH4 B.H2NOCCH2CH2CONH2
C.HOCH2CH2OH D.HOCH2CH2NH2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com