
(14分)研究银及其化合物具有重要意义。
(l)已知:
Ag2O(s)+2HC1(g) 2AgC1(s)+H2O(1) △H1=-324.4 kJ·mo1-1
2Ag(s)+1/2O2(g) Ag2O(s) △H2=-30.6 kJ·mo1-1
H2(g)+C12(g) 2HC1(g) △H3=-184.4 kJ.·mo1-1
2H2(9)+O2(g) 2H2O(1) △H4=-571.2 l·mo1-1
写出氯气与银生成固体氯化银的热化学方程式________。
(2)美丽的银饰常用Fe(NO3)3溶液蚀刻,写出Fe3+与Ag反应的离子方程式___ _;要判定Fe(NO3)3溶液中NO3—是否在银饰蚀刻中发生反应,可取 的硝酸溶液,然后根据其是否与Ag发生反应来判定。
(3)银锌碱性电池的电解质溶液为KOH溶液,放电时,正极Ag2O2转化为Ag,负极Zn转化为Zn(OH)2,则正极反应式为 ,负极附近溶液的pH ___ (填“增大”、“不变”或“减小”)。
(4)电解法精炼银时,粗银应与直流电源的 极相连,当用AgNO3和HNO3混合溶液做电解质溶液时,发现阴极有少量红棕色气体,则产生该现象的电极反应式为____。
(l)2Ag(s)+C12(g) 2AgC1(s)△H=-253.8 kJ·mo1-1;
(2)Fe3++Ag Fe2++Ag+;与Fe(NO3)3溶液pH相同或与Fe(NO3)3溶液H+浓度相同;
Fe2++Ag+;与Fe(NO3)3溶液pH相同或与Fe(NO3)3溶液H+浓度相同;
(3)Ag2O2+4e-+2H2O=2Ag+4OH-,减小;
(4)正极,2H++NO3-+e-=NO2↑+H2O。
解析试题分析:(l)已知:①Ag2O(s)+2HC1(g) 2AgC1(s)+H2O(1) △H1=-324.4 kJ·mo1-1
②2Ag(s)+1/2O2(g) Ag2O(s) △H2=-30.6 kJ·mo1-1
③H2(g)+C12(g) 2HC1(g) △H3=-184.4 kJ.·mo1-1
④2H2(g)+O2(g) 2H2O(1) △H4=-571.2 l·mo1-1
根据盖斯定律:①+②+③+④×1/2得氯气与银生成固体氯化银的热化学方程式
2Ag(s)+C12(g) 2AgC1(s)△H=-253.8 kJ·mo1-1。
(2)Fe3+与Ag反应生成亚铁离子和银离子,离子方程式为Fe3++Ag Fe2++Ag+;Fe(NO3)3溶液水解显酸性,硝酸根离子在酸性溶液中具有氧化性,可以与银发生氧化还原反应,要判定Fe(NO3)3溶液中NO3—是否在银饰蚀刻中发生反应,可取与Fe(NO3)3溶液pH相同或与Fe(NO3)3溶液H+浓度相同的硝酸溶液,然后根据其是否与Ag发生反应来判定。
Fe2++Ag+;Fe(NO3)3溶液水解显酸性,硝酸根离子在酸性溶液中具有氧化性,可以与银发生氧化还原反应,要判定Fe(NO3)3溶液中NO3—是否在银饰蚀刻中发生反应,可取与Fe(NO3)3溶液pH相同或与Fe(NO3)3溶液H+浓度相同的硝酸溶液,然后根据其是否与Ag发生反应来判定。
(3)银锌碱性电池的电解质溶液为KOH溶液,放电时,正极Ag2O2转化为Ag,负极Zn转化为Zn(OH)2,根据原子守恒和电荷守恒可得正极电极反应式为Ag2O2+4e-+2H2O=2Ag+4OH-,负极电极反应式为2Zn-4e-+4OH-=2Zn(OH)2,根据电极反应式知,负极附近氢氧根离子浓度减小,溶液的pH减小;
(4)迁移教材铜的电解精炼知识知,电解法精炼银时,纯银作阴极,粗银作阳极,应与直流电源的正极相连,当用AgNO3和HNO3混合溶液做电解质溶液时,发现阴极有少量红棕色气体,说明阴极上硝酸根离子得电子生成二氧化氮,电极反应式为:2H++NO3-+e-=NO2↑+H2O。
考点:考查热化学方程式书写和盖斯定律、离子方程式书写、实验方案的设计、原电池原理和化学电源、电解原理的应用、电极方程式的书写。


 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:填空题
(1)、①用肼(N2H4)为燃料,四氧化二氮做氧化剂,两者反应生成氮气和气态水。
已知:N2(g)+2O2(g)=N2O4(g) ΔH=+10.7kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543kJ·mol-1
写出气态肼和N2O4反应的热化学方程式: 。
②已知四氧化二氮在大气中或在较高温度下很难稳定存在,其很容易转化为二氧化氮。试推断由二氧化氮制取四氧化二氮的反应条件(或措施): 。
(2)科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。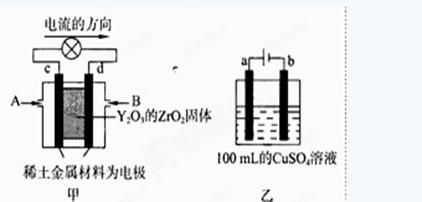
图甲所示装置中,以稀土金属材料为惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-(O2+4e →2O2-)
①c电极为 ,d电极上的电极反应式为 。
②图乙是电解100mL 0.5mol·L-1 CuSO4溶液,a电极上的电极反应式为 。若a电极产生56mL(标准状况)气体,则所得溶液的pH= (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入 (选填字母序号)
a.CuO b.Cu(OH)2 c.CuCO3 d.Cu2(OH)2CO3
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
合成氨工业对国防具有重要意义,如制硝酸、合成纤维以及染料等
(1)已知某些化学键的键能数据如下表:
| 化学键 | N≡N | H—H | N—H |
| 键能kJ·mol-1 | 946 | 436 | 390 |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(15分)A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题: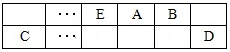
(1)A元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为 。
(2)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若所得溶液的pH=7,则a b(填“>"或“<”或“=”)
(3)常温下,相同浓度F、G简单离子的溶液中滴加NaOH溶液,F、G两元素先后沉淀,F (OH)n完全沉淀的pH是4.7,G (OH)n完全沉淀的pH是2.8,则ksp较大的是: (填化学式)
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有: 。
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)A和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是 。
(6)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如下左图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式 。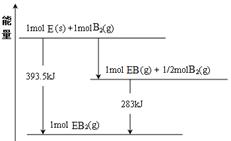
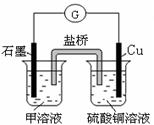
(7)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如上右图所示,其反应中正极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(12分) (1)已知:蒸发1 mol Br2(l)需要吸收的能量为 30 kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1 mol分子中化学键断裂时需要吸收的能量/kJ | 436 | 200 | 369 |
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
(14分)硫化物在自然界中的部分循环关系如下。
(1)H2S在空气中可以燃烧。
已知: 2H2S(g) + O2(g)  2S(s) + 2H2O(g) ΔH= -442.38 kJ/mol ①
2S(s) + 2H2O(g) ΔH= -442.38 kJ/mol ①
S(s) + O2(g)  SO2(g) ΔH=-297.04 kJ/mol ②
SO2(g) ΔH=-297.04 kJ/mol ②
H2S(g)与O2(g)反应产生SO2(g)和H2O(g)的热化学方程式是 。
(2)SO2是大气污染物,海水具有良好的吸收SO2的能力,其过程如下。
① SO2溶于海水生成H2SO3,H2SO3最终会电离出SO32—,其电离方程式是 。
② SO32—可以被海水中的溶解氧氧化为SO42—。海水的pH会 (填“升高” 、“不变”或“降低”)。
③ 为调整海水的pH,可加入新鲜的海水,使其中的HCO3—参与反应,其反应的离子方程式是 。
④ 在上述反应的同时需要大量鼓入空气,其原因是 。
(3)自然界地表层原生铜的硫化物经氧化、淋滤作用后变成CuSO4溶液,向地下深层渗透,遇到难溶的ZnS,慢慢转变为铜蓝(CuS),用化学用语表示由ZnS转变为CuS的过程: 。
(4)SO2和O2在H2SO4溶液中可以构成原电池,其负极反应式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:问答题
依据事实,写出下列反应的热化学方程式。
(1)1molC2H4(g)与适量O2(g)反应生成CO2(g)和H2O(l),放出1411kJ热量。
(2)1molC2H5OH(l)与适量O2(g)反应生成CO2(g)和H2O(l),放出1366.8kJ热量。
(3)2molAl(s)与适量O2(g)反应生成Al2O3(s),放出1669.8kJ热量。
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
多晶硅(硅单质的一种)被称为“微电子大厦的基石”,制备中副产物以SiCl4为主,它环境污染很大,能遇水强烈水解,放出大量的热。研究人员利用SiCl4水解生成的盐酸和钡矿粉(主要成分为BaCO3,且含有铁、镁等离子)制备BaCl2·2H2O,工艺流程如下: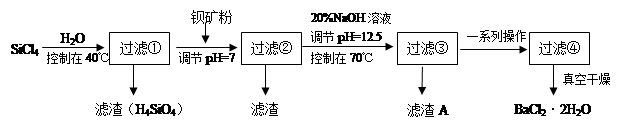
已知:
①常温下Fe3+、Mg2+完全沉淀的pH分别是3.4、12.4
②BaCO3的相对分子质量是197;BaCl2·2H2O的相对分子质量是244
回答下列问题:
(1)SiCl4发生水解反应的化学方程式为_______________________________________
(2)用H2还原SiCl4蒸汽可制取纯度很高的硅,当反应中有1mol电子转移时吸收59KJ热量,则该反 应的热化学方程式为_____________________________________________
(3)加钡矿粉并调节pH=7的目的是① ,②
(4)过滤②后的滤液中Fe3+浓度为 (滤液温度25℃,Ksp[Fe(OH)3]=2.2×10-38)
(5)生成滤渣A的离子方程式__________________________________________
(6)列式计算出10吨含78.8% BaCO3的钡矿粉理论上最多能生成BaCl2·2H2O的质量为多少吨?
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2。下列关于此反应的说法中,正确的是
| A.减小压强能增大反应速率 | B.增大压强能减小反应速率 |
| C.使用适当的催化剂能增大反应速率 | D.升高温度对反应速率无影响 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com