
【题目】一定条件下,草酸铜晶体(CuC2O4· xH2O)受热分解的化学方程式为: CuC2O4· xH2O·![]() CuO+CO↑ +CO2↑ +xH2O↑。某化学兴趣小组设计如图装置,探究草酸铜晶体分解的气体产物:
CuO+CO↑ +CO2↑ +xH2O↑。某化学兴趣小组设计如图装置,探究草酸铜晶体分解的气体产物:
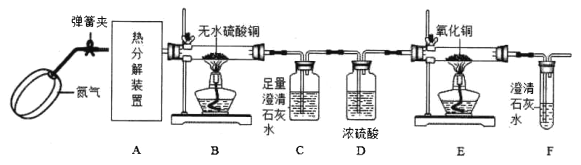
请回答:
(1)该套实验装置的明显缺陷是________。
(2)实验过程中观察到B中白色无水硫酸铜变成蓝色,C、F中澄清石灰水变浑浊,E中________ (填实验现象),则可证明草酸铜晶体热分解的气体产物是H2O、CO、CO2。
(3)该兴趣小组改变热分解反应条件,完全反应后发现C中白色沉淀量明显较先前实验多,而E、F中未见明显现象,请推测A装置中固体产物成分并设计一个实验方案,用化学方法验证固体产物________ (不考虑操作和药品的问题)。
【答案】 没有尾气处理装置 黑色粉末变红色 固体产物为Cu单质;取少量受热分解后固体产物,加入适量稀硫酸,未见溶液呈蓝色,则证明推测合理
【解析】(1)由装置图结合分解产物可知,B装置用于检验有水生成,C装置用于检验有CO2生成,D装置用于干燥CO气体,E装置用于检验有CO生成,F装置用于吸收E中生成的CO2,但在E中CO不可能完全反应,所以这套装置中没有处理尾气CO的装置;
(2)E装置是用CO还原CuO,所以现象是黑色粉末变红色;
(3)由于改变了反应条件,可能使分解生成的CO直接把CuO还原为Cu单质,这样没有CO与E中的CuO反应,所以E、F中都没有明显现象,所以A装置中固体产物为铜单质,检验的化学方法是取少量受热分解后固体产物,加适量稀硫酸,未见溶液呈蓝色,则证明上述推测是合理的。


科目:高中化学 来源: 题型:
【题目】下列行为中符合安全要求的是( )
A.进入煤矿井时,用火把照明
B.实验时,将水倒入浓硫酸配制稀硫酸
C.用点燃的火柴在液化气钢瓶口检验是否漏气
D.节日期间,在开阔的广场燃放烟花爆竹
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物A经李比希法测得其中含碳为72.0%、含氢为6.67%,其余为氧。现用下列方法测定该有机化合物的相对分子质量和分子结构。
方法一:用质谱法分析得知A的相对分子质量为150。
方法二:核磁共振仪测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3,如下图所示。
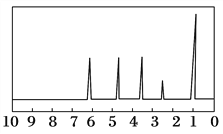
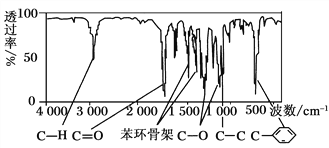
方法三:利用红外光谱仪测得A分子的红外光谱如上图所示。
请填空:
(1)A的分子式为________。
(2)A的分子中含一个甲基的依据是________。
a.A的相对分子质量 b.A的分子式
c.A的核磁共振氢谱图 d.A分子的红外光谱图
(3)A的结构简式为________。
(4)A的芳香类同分异构体有多种,其中符合下列条件:①分子结构中只含一个官能团;②分子结构中含有一个甲基;③苯环上只有一个取代基。则该类A的同分异构体共有________种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组查阅资料得知工业上常采用蒽醌法生产 H2O2,其原理与流程如图所示:
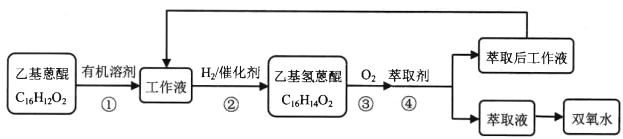
下列说法不正确的是
A. 蒽醌法制备 H2O2理论上消耗的原料是H2、O2,乙基蒽醌可循环使用
B. 步骤②为还原反应,步骤③为氧化反应
C. 步骤④中可选用 CCl4作为萃取剂
D. 应除净萃取后工作液残留的H2O2,否则释放的氧气与氢气混合易爆炸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】V L浓度为1.000 mol·L-1的盐酸,欲使其浓度增大1倍,采取的措施合理的是
A. 向原溶液中通入常温常压下的HCl气体22.4V L,使其完全溶解
B. 将溶液加热浓缩到0.5V L
C. 向原溶液中加入10.00 mol·L-1的盐酸0.2V L,再稀释至1.5V L
D. 向原溶液中加入V L 3 mol·L-1的盐酸混合均匀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.离子反应和氧化还原反应都是高中化学中重要的反应类型。回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在有______。(填序号)
①单质 ②化合物 ③氧化物 ④酸 ⑤碱 ⑥盐 ⑦电解质
人们常用图示法表示不同反应类型之间的关系,如化合反应和氧化还原反应的关系可用图1表示。图2为离子反应、氧化还原反应和置换反应三者之间的关系,则表示置换反应的是____(填字母),请写出符合图2阴影部分的一个离子方程式______。


图1 图2
Ⅱ.现有失去标签的四瓶无色溶液A,B,C,D,只知它们是K2CO3,K2SO4,Na HSO4和Ba(NO3)2,为鉴别它们,进行如下实验:
①A+D→溶液+气体 ②B+C→溶液+沉淀
③B+D→溶液+沉淀 ④A+B→溶液+沉淀
⑤将④得到的沉淀物加入③所得的溶液中,沉淀很快溶解并产生无色无味的气体。
根据以上实验事实,请完成如下问题:
(3)写出各物质化学式:A__________;B__________;C__________;D__________。
(4)写出实验③中反应中相关的离子方程式。____________________________。
(5)书写离子方程式
①NaHCO3溶液与H2SO4溶液混合:_________________________。
②向石灰水中通入过量二氧化碳________________________________。
③氢氧化亚铁和浓盐酸反应____________________________________。
④醋酸溶液和碳酸镁悬浊液混合生成气体并得到澄清溶液______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组变化中,化学反应的反应热前者大于后者的一组是( )
①CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H1; CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H2;
②2H2(g)+O2(g)=2H2O(l)△H1; H2(g)+O2(g)=H2O(l)△H2
③t℃时,在一定条件下,将1molSO2和1molO2混合后,分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为Q1、Q2
④CaCO3(s)=CaO(s)+CO2(g)△H1;CaO(s)+H2O(l)=Ca(OH)2(s)△H2
A. ①③④ B. ②③ C. ①④ D. ①②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为 “零号元素”。下列有关“四中子”粒子的说法不正确的是( )
A.该粒子不显电性B.该粒子质量数为 4
C.在周期表中与氢元素占同一位置D.该粒子质量比氢原子大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com