
【题目】回答下面问题:
(1)在①KNO3 ②K2CO3 ③(NH4)2SO4 三种盐溶液中,常温下呈酸性的是_____(填序号),显酸性的原因是_____(用化学用语表示)。
(2)将三氯化锑(SbCl3)固体溶于水,生成白色沉淀,且溶液 pH<7,则配制 SbCl3 溶液的正确方法是_____
(3)某温度下,向含有 AgCl 固体的 AgCl 饱和溶液中加入少量稀盐酸,则 c(Ag+)_____(填“增大”“减小”或“不变”,下同),Ksp_____。
【答案】③ NH![]() +H2O
+H2O![]() NH3H2O+H+ 先将SbCl3加入到较浓的盐酸中,搅拌溶解,再稀释成需要的浓度 减小 不变
NH3H2O+H+ 先将SbCl3加入到较浓的盐酸中,搅拌溶解,再稀释成需要的浓度 减小 不变
【解析】
(1)①KNO3是强酸强碱盐,呈中性,②K2CO3是强碱弱酸盐,呈碱性,③(NH4)2SO4是强酸弱碱盐,呈酸性,所以呈酸性的是③,显酸性的原因NH![]() 水解,水解方程式为NH
水解,水解方程式为NH![]() +H2O
+H2O![]() NH3H2O+H+;
NH3H2O+H+;
(2)三氯化锑(SbCl3)固体溶于水,生成白色沉淀,且溶液pH<7,是由于三氯化锑发生了水解,可以加入盐酸抑制水解的发生,则配制SbCl3溶液的正确方法是先将SbCl3加入到较浓的盐酸中,搅拌溶解,再稀释成需要的浓度;
(3)在含AgCl固体的AgCl饱和溶液中存在沉淀溶解平衡:AgCl(s)![]() Ag+(aq)+Cl-(aq),当加入少量稀盐酸时,c(Cl-)增大,平衡逆向移动,c(Ag+)减小;AgCl的Ksp只受温度影响,温度不变,AgCl的Ksp不变。
Ag+(aq)+Cl-(aq),当加入少量稀盐酸时,c(Cl-)增大,平衡逆向移动,c(Ag+)减小;AgCl的Ksp只受温度影响,温度不变,AgCl的Ksp不变。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列实验中的操作,对应的现象以及结论都正确的是![]()
![]()
选项 | 操作 | 现象 | 结论 |
A | 向 | 产生白色沉淀 |
|
B | 蘸有浓氨水的玻璃捧靠近X | 有白烟产生 | X一定是浓盐酸 |
C | 向澄清石灰水加入某试剂的溶液少许 | 产生白色沉淀 | 该试剂中一定含有 |
D | 炭粉中加入浓硫酸并加热,导出的气体通入 | 有白色沉淀产生 | 有 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
A. 在常温常压下,11.2 L N2含有的原子数为NA
B. 32 g O2在标准状况下所占体积约为22.4 L
C. 标准状况下,18 g H2O所占的体积约为22.4 L
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若它们的温度和密度均相同,试根据甲、乙的摩尔质量![]() 关系,判断下列说法正确的是( )
关系,判断下列说法正确的是( )
A.若![]() ,则气体的压强:甲
,则气体的压强:甲![]() 乙
乙
B.若![]() ,则气体的摩尔体积:甲
,则气体的摩尔体积:甲![]() 乙
乙
C.若![]() ,则气体体积:甲
,则气体体积:甲![]() 乙
乙
D.若![]() ,则分子数:甲
,则分子数:甲![]() 乙
乙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定稳定下,在容积不变的密闭容器中,进行如下可逆反应:![]() ,下列能表明该反应已达到平衡状态的是
,下列能表明该反应已达到平衡状态的是
①![]()
②![]()
③![]()
④混合气的密度保持不变
⑤混合气体的平均摩尔质量不变
A.仅④B.仅④⑤
C.仅①④D.仅③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验的现象、解释或结论正确的是( )
选项 | 实验 | 解释或结论 |
A | 向某溶液中逐渐通入CO2气体,先出现白色胶状沉淀,继续通入CO2气体,白色胶状沉淀不溶解,证明该溶液中存在AlO2- | Al(OH)3是两性氢氧化物,不溶于碳酸溶液 |
B | 在新制氯水中加入碳酸钙粉末,充分搅拌,氯水的漂白性增强 | 氯水中HClO的物质的量浓度增大 |
C | 用蒸馏法能将溶解在CCl4中的碘分离出来 | 因为碘易升华,先分离出来 |
D | 向Fe(NO3)2溶液中滴入硫酸酸化的H2O2溶液,则溶液变为黄色 | 氧化性:H2O2 > Fe3+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )

A.该实验说明氨气是一种极易溶于水的气体
B.进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性
C.氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化
D.形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸盐在能源、环保等方面有着广泛的用途,在生产和生活中有广泛的应用。
已知:i.高铁酸钠(Na2FeO4)极易溶解于水,20℃溶解度为111克;高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。
ii.高铁酸钾(K2FeO4)在中性或酸性溶液中逐渐分解,在碱性溶液中稳定。
iii.高铁酸根在水溶液中存在平衡:![]()
![]() ↑
↑
(1)工业上用氯气和烧碱溶液可以制取次氯酸钠,反应的离子方程式为___________。
(2)高铁酸钾是一种理想的水处理剂,既可以对水杀菌消毒,又可以净化水,其原理为________。
(3)工业上有多种方法制备高铁酸钾。
方法1:次氯酸盐氧化法。工艺流程如图所示。
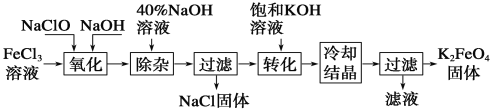
①“氧化”过程中的氧化剂为(填化学式)______________。
②写出“转化”过程中的化学方程式为__________________。
③上述工艺得到的高铁酸钾常含有杂质,可用重结晶法提纯,操作是将粗产品先用稀KOH溶液溶解,然后再加入饱和KOH溶液,冷却结晶过滤。上述操作中溶解粗产品用稀KOH溶液,不用蒸馏水,根据平衡移动原理解释__________。
(4)方法2:电解法
我国化学工作者还提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如下图所示。
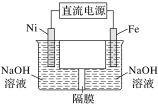
①Ni电极作________(填“阴”或“阳”)极;
②Fe电极的电极反应式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于实验的描述不正确的是( )
A.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度偏低
B.过滤时,玻璃棒靠在三层滤纸边沿稍下方
C.在镀件上电镀铜时,可用金属铜作阳极
D.在用Fe(OH)3胶体溶液做电泳实验时,阴极区红色加深,可知Fe(OH)3胶体粒子带正电荷
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com