
| X | Y | W | |
| n����ʼ״̬��/mol | 2 | 1 | 0 |
| n��ƽ��״̬��/mol | 1 | 0.5 | 1.5 |
| A�� | �˷�Ӧ��ƽ�ⳣ������ʽ��K=$\frac{{c}^{2}��X��•c��Y��}{{c}^{3}��W��}$ | |
| B�� | �ﵽƽ��������¶ȣ�W������������٣���˷�Ӧ�ġ�H��0 | |
| C�� | �ﵽƽ�������ѹǿ�������淴Ӧ���ʾ�����ƽ��������Ӧ�����ƶ� | |
| D�� | �ﵽƽ����������ѹ��Ϊ2L��W�����ʵ���Ũ�ȱ�Ϊ0.75mol•L-1 |
���� �ɱ������ݿ�֪��X��YΪ��Ӧ�WΪ����������ʵ����仯��֮��Ϊ��2-1������1-0.5����1.5=2��1��3����ӦΪ2X+Y?3W��
A��KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ�
B�������¶ȣ�W������������٣���֪�����¶�ƽ�������ƶ���
C���÷�ӦΪ�����������ķ�Ӧ������ѹǿ�������淴Ӧ����ͬ�ȳ̶�����
D���ﵽƽ����������ѹ��Ϊ2L��ƽ�ⲻ�ƶ���
��� �⣺�ɱ������ݿ�֪��X��YΪ��Ӧ�WΪ����������ʵ����仯��֮��Ϊ��2-1������1-0.5����1.5=2��1��3����ӦΪ2X+Y?3W��
A��KΪ������Ũ����֮���뷴Ӧ��Ũ����֮���ıȣ���ƽ�ⳣ������ʽ��K=$\frac{{c}^{3}��W��}{{c}^{2}��X��c��Y��}$����A����
B�������¶ȣ�W������������٣���֪�����¶�ƽ�������ƶ�������ӦΪ���ȷ�Ӧ�����H��0����B����
C���÷�ӦΪ�����������ķ�Ӧ������ѹǿ�������淴Ӧ����ͬ�ȳ̶�����ƽ�ⲻ�ƶ�����C����
D���ﵽƽ����������ѹ��Ϊ2L��ƽ�ⲻ�ƶ���W�����ʵ���Ũ�ȱ�Ϊ$\frac{1.5mol}{2L}$=0.75mol•L-1����D��ȷ��
��ѡD��
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬���շ�Ӧ������P����ʽ��ȷ����K�ı���ʽ��ƽ���ƶ�Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��ƽ���ƶ�ԭ����Ӧ�ã���Ŀ�ѶȲ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ʱ��/min | 0 | 10 | 20 | 40 | 50 | |
| T1 | n��CH4��/mol | 1.00 | 0.70 | 0.50 | 0.20 | 0.20 |
| T2 | n��CH4��/mol | 1.00 | 0.60 | 0.36 | �� | 0.30 |
| A�� | T2ʱNO2��ƽ��ת����Ϊ70.0% | |
| B�� | �÷�Ӧ�ġ�H��0��T1��T2 | |
| C�� | ���������������䣬T1ʱ��ƽ����ϵ���ٳ���1.00molCH4��2.40molNO2����ԭƽ����ȣ�����ƽ��ʱN2��Ũ���������������С | |
| D�� | ���������������䣬T1ʱ��ƽ����ϵ���ٳ���0.60molCH4��1.60molH2O��g����ƽ��������Ӧ�����ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
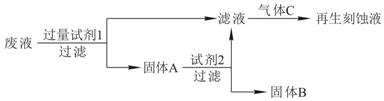
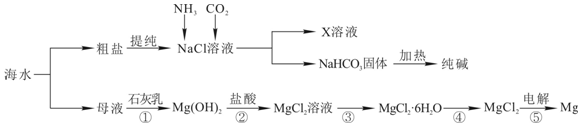
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ������ | �� | �� | �� | |
| A | �� | ˮ | ���� | С�մ� | ���� |
| B | ���� | ������ | H2SiO3 | KOH | NH4Cl |
| C | ����� | �������� | ���� | '���� | ���� |
| D | Һ�� | ���� | ���� | Ca��OH��2 | Na2SO4 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ȼ����Ϊ285.5 kJ•mol-1����ˮ�ֽ���Ȼ�ѧ����ʽΪ2H2O��l���T2H2��g��+O2��g����H=+285.5 kJ•mol-1 | |
| B�� | ��֪2C��ʯī��s��+O2��g���T2CO��g����H=-221 kJ•mol-1����ʯī��ȼ����Ϊ 110.5 kJ•mol-1 | |
| C�� | ��֪N2��g��+3H2��g��?2NH3��g����H=-92.4 kJ•mol-1������һ�������½�1 mol N2��3 mol H2����һ�ܱ������г�ַ�Ӧ�����ɷų�92.4 kJ������ | |
| D�� | ��֪�Ҵ�����ϩ��ȼ���ȷֱ�Ϊ1 366.8 kJ•mol-1��1 411.0 kJ•mol-1������ϩˮ�����Ҵ����Ȼ�ѧ����ʽΪC2H4��g��+H2O��l���TC2H5OH��l����H=-44.2 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | �Ҵ� | B�� | ���� | C�� | ��ϩ | D�� | �� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1.0��10-7 mol/L | B�� | 1.0��107 mol/L | C�� | $\frac{0.1}{a}$mol/L | D�� | $\frac{0.1b}{a+b}$mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �ƹ������ʹ�ù�����ͨ���߳��� | |
| B�� | ֲ�����֣��̻����� | |
| C�� | ��������ú̿��������չ�������� | |
| D�� | ��ȼú���������ٿ�������Ⱦ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com