
【题目】
两名日本科学家与一名美国科学家利用钯作催化剂,将有机物进行“裁剪”、“缝合”,创造出具有特殊功能的新物质而获2010年诺贝尔化学奖。下列说法正确的是( )
A. 有机物中一定含有碳和氢两种元素
B. 一定条件下,使用催化剂能提高反应的平衡转化率
C. 将有机物进行“缝合”可以不遵循原子守恒定律
D. 将有机物进行“裁剪”需要破坏旧的化学键
科目:高中化学 来源: 题型:
【题目】NaClO2是一种重要的杀菌消毒剂,也常用来漂白织物等,同时也是对烟气进行脱硫、脱硝的吸收剂。其一种生产工艺如下:

已知:
纯ClO2易分解爆炸,空气中 ClO2的体积分数在 10%以下比较安全;
NaClO2在碱性溶液中稳定存在,在酸性溶液中迅速分解;
NaClO2饱和溶液在温度低于 38℃时析出 NaClO23H2O,等于或高于38℃时析出 NaClO2,高于 60℃时分解成 NaClO3和 NaCl。回答下列问题:
(1)写出“反应”步骤中生成 ClO2的化学方程式_________。
(2)从滤液中得到的 NaClO23H2O 晶体的方法是_________。
(3)“尾气吸收”是吸收“电解”过程排出的少量 ClO2 。在尾气吸收过程中,可代替 H2O2的试剂是_________(填序号)。
A.Na2O2 B.Na2S C.FeCl2 D.KMnO4
(4)国家标准规定产品中优级纯试剂纯度≥99.8%,分析纯试剂纯度≥99.7%,化学纯试剂纯度≥99.5%。为了确定某批次 NaClO2产品的等级,研究小组设计测定方案如下:取 10.00g 样品,用适量蒸馏水溶解后,加入略过量的 KI 溶液;充分反应后,将反应液定容至 200mL, 取出 20.00mL 于锥形瓶;向锥形瓶中滴加两滴淀粉溶液,用 2.00molL﹣1的 Na2S2O3溶液与之反应,消耗Na2S2O3溶液 22.00mL。该样品可达试剂纯度 ________________。(写出计算过程) 已知: ClO2﹣+4I﹣+4H+═2H2O+2I2+Cl﹣ , I2+2S2O32﹣═2I﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫化氢中的硫元素化合价为______,在化学反应中易_____(填得或失)电子,因此具有______性。硫化氢可燃,氧气充足情况下,硫化氢燃烧产生淡蓝色火焰,化学方程式_________;氧气不足情况下,硫化氢燃烧化学方程式_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F(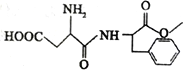 )是一种应用广泛可食用的甜味剂,俗称蛋白糖,它的一种合成路线如图所示
)是一种应用广泛可食用的甜味剂,俗称蛋白糖,它的一种合成路线如图所示

已知:①A能发生银镜反应
②
③R-CN![]() R-COOH
R-COOH
请回答下列问题:
(1)D中官能团的名称为___________,F的分子式为___________。
(2)A的名称为___________,反应③的反应类型为___________。
(3)反应④的化学方程式为___________。
(4)反应⑤中的另一种生成物是水,则X的结构简式为___________。
(5)D有多种同分异构体,请写出一种符合下列条件的有机物的结构简式___________;
①苯环上有2个取代基
②与D具有相同的官能团
③核破共振氢谱为6组峰且峰面积比为2:2:2:2:2:1
(6)丙烯酸是重要的有机合成原料及合成树脂单体,请写出以CH3CHO为原料合成丙烯酸的合成路线___________(其它试剂任选)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电池是人类生产和生活中的重要能量来源,下列有关电池的叙述正确的是( )
A. 锌锰干电池工作一段时间后碳棒变细
B. 铅蓄电池放电时铅在负极被氧化成二氧化铅
C. 太阳能电池的主要材料是高纯度的二氧化硅
D. 氢氧燃料电池产物为水,属于环境友好电池
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用_______和_______作为原料来制取漂粉精,反应的化学方程式为_______;粉精长期暴露在空气中,会使其失效,主要化学方程式__________;______________________,故其应_______保存。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】叠氮化钠(NaN3)固体易溶于水,微溶于乙醇,不溶于乙醚,是汽车安全气囊中的主要成分,能在发生碰撞的瞬间分解产生大量气体将气囊鼓起。
已知:①NaNH2+N2O![]() NaN3+H2O。
NaN3+H2O。
②NaNH2能与水反应生成NaOH和NH3
实验室利用如下装置模拟工业级NaN3的制备。

请回答下列问题:
实验I:制备NaN3
(1)装置C中盛放的药品为______________________;
(2)为了使反应均匀受热,装置D处b容器应采取的加热方式为______________________。
(3)实验开始时首先应加热通氨气,其目的是___________。
(4)氨气与熔化的钠反应生成NaNH2的化学方程式为___________。
实验Ⅱ:分离提纯
反应完全结束后,取出装置D中的混合物进行以下操作,得到NaN3固体。

(5)操作ⅳ采用乙醚洗涤的原因是______________________(答一项即可)。
实验Ⅲ:定量测定
实验室用滴定法测定叠氮化钠样品中NaN3的质量分数:
①将2.500g试样配成500mL溶液
②取50.00L溶液置于锥形瓶中,加入50.00mL0.1010m1·L-1(NH4)2Ce(NO3)6溶液。
③充分反应后,将溶液稍稀释,向溶液中加入8.00mL浓硫酸,滴人3滴邻菲啰啉指示液,用0.0500mol·L-1(NH4)2Fe(SO4)2标准溶液滴定过量的Ce4+,消耗溶液体积为29.00mL。测定过程的反应方程式为:2(NH4)2Ce(NO3)6+2NaN3=4NH4NO3+2Ce(NO3)3+2NaNO3+3N2↑, Ce4++Fe2+=Ce3++Fe3+。
(6)配制叠氮化钠溶液时,除需用到烧杯、玻璃棒、量筒外,还用到的玻璃仪器有______________________。
(7)若其它读数正确,滴定到终点后,读取滴定管中(NH4)2Fe(SO4)2标准溶液体积时俯视,将导致所测定样品中叠氮化钠质量分数___________(选填“偏大”、“偏小”或“不变”)。
(8)减样中NaN3的质量分数为___________ (保留四位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳、氮、硫是中学化学重要的非金属元素,在工农业生产中有广泛的应用。
![]() 与镍反应会造成含镍催化剂的中毒。为防止镍催化剂中毒,工业上常用
与镍反应会造成含镍催化剂的中毒。为防止镍催化剂中毒,工业上常用![]() 将CO氧化,二氧化硫转化为单质硫。
将CO氧化,二氧化硫转化为单质硫。
已知:![]()
![]()
![]()
![]()
![]()
则![]() ______
______![]() ;
;
![]() 时,在2L密闭容器中发生可逆反应:
时,在2L密闭容器中发生可逆反应:![]()
![]()
![]() ,
,![]() 的物质的量浓度随时间变化如图所示。达平衡时,
的物质的量浓度随时间变化如图所示。达平衡时,![]() 的浓度为
的浓度为![]() 的2倍,回答下列问题。
的2倍,回答下列问题。

![]() 时,该反应的平衡常数为
时,该反应的平衡常数为![]() 精确到小数点后两位
精确到小数点后两位![]() ______。
______。
![]() 在温度为
在温度为![]() 、
、![]() 时,平衡体系中
时,平衡体系中![]() 的体积分数随压强变化曲线如图所示。
的体积分数随压强变化曲线如图所示。

下列说法正确的是______
![]() 、C
、C![]()
![]() 、C两点气体的颜色:A深,C浅
、C两点气体的颜色:A深,C浅
![]() 由状态B到状态A,可以用加热的方法
由状态B到状态A,可以用加热的方法
![]() 若反应在398K进行,某时刻测得
若反应在398K进行,某时刻测得![]() ,
,![]() ,则此时
,则此时![]() ______
______![]() 填“
填“![]() ”、“
”、“![]() ”或“
”或“![]() ”
”![]()
![]() 在分析试剂、电子工业中用途广泛。现向100mL
在分析试剂、电子工业中用途广泛。现向100mL![]() 溶液中滴加
溶液中滴加![]() 溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,
溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图所示。试分析图中a、b、c、d、e五个点,

![]() 水的电离程度最大的是______;
水的电离程度最大的是______;
![]() 其溶液中
其溶液中![]() 的数值最接近
的数值最接近![]() 的电离常数K数值的是______。
的电离常数K数值的是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com