
【题目】某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32﹣、SO42﹣、NO3﹣中的几种.①若加入锌粒,产生无色无味无毒的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀的物质的量与加入NaOH的物质的量之间的关系如右图所示.则下列说法正确的是( ) 
A.溶液中的阳离子只有H+、Mg2+、Al3+
B.溶液中一定不含CO32﹣ , 一定含有SO42﹣和NO3﹣
C.溶液中n(NH4+)=0.2 mol
D.三种离子的物质的量之比n(H+):n(Al3+):n(Mg2+)=1:1:1
【答案】C
【解析】解:若加入锌粒,产生无色无味无毒的气体,说明气体是氢气,因此溶液显酸性,则CO32﹣和NO3﹣不能大量共存;
加入NaOH溶液,产生白色沉淀,说明不存在Fe3+;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,溶液中一定含有Mg2+、Al3+;又因为当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+ , 由于溶液中还必须存在阴离子,所以一定还有SO42﹣;
由图象可知,第一阶段为氢离子与氢氧化钠反应,消耗氢氧化钠为0.1mol,则n(H+)=0.1mol;
第三阶段为铵根离子与氢氧化钠反应,消耗氢氧化钠为0.7mol﹣0.5mol=0.2mol,则n(NH4+)=0.2mol;
最后阶段为氢氧化钠溶解氢氧化铝,消耗氢氧化钠0.8mol﹣0.7mol=0.1mol,则n[Al(OH)3]=0.1mol,根据铝元素守恒可知n(Al3+)=0.1mol;
第二阶段为氢氧化钠沉淀镁离子、铝离子,共消耗氢氧化钠为0.5mol﹣0.1mol=0.4mol,则n(Mg2+)=(0.4mol﹣0.1mol×3)÷2=0.05mol,
A.由上述分析可知,溶液中的阳离子只有H+、Mg2+、Al3+、NH4+ , 故A错误;
B.由上述分析可知,溶液中一定不含CO32﹣、NO3﹣ , 一定含有SO42﹣ , 故B错误;
C.由上述分析可知,溶液中n(NH4+)=0.2mol,故C正确;
D.由上述分析可知,溶液中n(H+):n(Al3+):n(Mg2+)=0.1mol:0.1mol:0.05mol=2:2:1,故D错误,
故选C.
若加入锌粒,产生无色无味无毒的气体,说明气体是氢气,因此溶液显酸性,则CO32﹣和NO3﹣不能大量共存;加入NaOH溶液,产生白色沉淀,说明不存在铁离子;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,溶液中一定含有Mg2+、Al3+;又因为当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+ , 由于溶液中还必须存在阴离子,所以一定还有SO42﹣ . 结合图象中各阶段消耗的氢氧化钠,计算溶液中n(H+)、n(Mg2+)、n(Al3+)、n(NH4+),据此解答.


科目:高中化学 来源: 题型:
【题目】按要求填空
(1)2017年1月2日安徽六安出现了严重雾霾情况,经分析该雾霾中含有大量PM2.5、PM10、汽车尾气等等.将PM2.5样本用蒸馏水处理制成待测试样.若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH4+ | SO42﹣ | NO3﹣ | Cl﹣ |
浓度/molL﹣1 | 4×10﹣6 | 6×10﹣6 | 2×10﹣5 | 4×10﹣5 | 3×10﹣5 | 2×10﹣5 |
根据表中数据判断PM2.5试样的pH= .
(2)在一定条件下的溶液中,反应FeCl3+3KSCNFe(SCN)3+3KCl达到平衡后,在其他条件不变的情况下,加入少量KCl固体,能使平衡移动(填“正向”、“逆向”、“不”)
(3)泡沫灭火器是硫酸铝和碳酸氢钠溶液反应,反应的离子方程式是 .
(4)常温下,一定体积PH=2的二元弱酸H2R溶液与等体积PH=12的NaOH溶液混合,该混合溶液中电荷守恒的关系式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面叙述正确的是( )
A.同质量的H2与Cl2 , H2的分子数一定比Cl2多
B.0.5mol氢的质量是0.5g
C.摩尔是用来衡量微观粒子多少的一种物理量
D.0.1mol H2SO4含有氢原子数的精确值为1.204×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1mol/L,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是( )

A. Ka(HA)=1×10-6mol/L
B. b点c (B+)=c(A-)=c(OH-)=c(H+)
C. c点时,![]() 随温度升高而减小
随温度升高而减小
D. a→c过程中水的电离程度始终增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含CuSO4和H2SO4的混合溶液200mL,其中CuSO4物质的量浓度为1molL﹣1 , H2SO4物质的量浓度为0.5molL﹣1 , 若用此溶液配成0.2molL﹣1 CuSO4和2molL﹣1 H2SO4的混合溶液,试求:
(1)所得溶液的体积是多少毫升?
(2)需加入密度为1.84gcm﹣3、98%的浓硫酸多少毫升?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.硫离子的结构示意图为 
B.核外电子排布相同的微粒化学性质也相同
C.氢弹中用到的2H,3H互为同位素
D.同种元素的原子均有相同的质子数和中子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一小块钠投入到盛有煤油和水的试管中(煤油和水均足够多),想一想可能观察到的现象是
A. 钠浮在试管的液面上 B. 钠沉入试管底部
C. 钠处于煤油和水的交界处 D. 钠燃烧起来
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】要检验己烯中是否混有少量甲苯,正确的实验方法是( )
A.先加足量的酸性高锰酸钾溶液,然后再滴加溴水
B.先加足量溴水,然后再滴加酸性高锰酸钾溶液
C.点燃这种液体,然后再观察火焰的颜色
D.加入浓硫酸与浓硝酸后加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应 A+B→C(△H<0)分两步进行 ①A+B→X (△H>0)②X→C(△H<0)下列示意图中,能正确表示总反应过程中能量变化的是( )
A.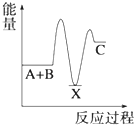
B.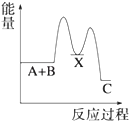
C.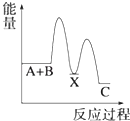
D.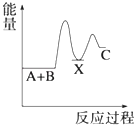
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com