
| A. | 由长、短周期元素共同组成的元素族称为主族 (除零族外) | |
| B. | 同一元素不可能既表现金属性,又表现非金属性 | |
| C. | 短周期元素原子形成简单离子后,最外层电子都达到8电子稳定结构 | |
| D. | 互为同位素的不同核素,物理性质和化学性质都不同 |
分析 A.由长、短周期元素共同组成的元素族称为主族 (除零族外);
B.位于金属与非金属交界处的元素通常具有一定的金属性、非金属性;
C.H原子形成的离子,最外层不满足8电子稳定结构;
D.互为同位素的元素,化学性质相同.
解答 解:A.由长、短周期元素共同组成的元素族称为主族 (除零族外),故A正确;
B.位于金属与非金属交界处的元素通常具有一定的金属性、非金属性,如Al、Si、Ge等,故B错误;
C.H原子形成的离子,最外层不满足8电子稳定结构,故C错误;
D.互为同位素的元素,物理性质不同,但化学性质相同,故D错误,
故选A.
点评 本题考查元素周期表的结构与应用,比较基础,注意掌握元素周期表中一些特殊性元素.


科目:高中化学 来源: 题型:选择题
| A. | 1.8mol | B. | <0.9mol | ||
| C. | 0.9mol | D. | 在0.9mol和1.8mol之间 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③⑤ | B. | ①⑥⑦ | C. | ②④⑦ | D. | ②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ③④ | C. | ④ | D. | ①②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X、Y、Z的浓度不再发生变化 | |
| B. | X、Y、Z三种物质体积分数均相等 | |
| C. | 气体总质量保持不变 | |
| D. | 单位时间消耗3molY,同时生成2molZ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
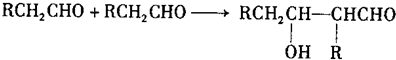
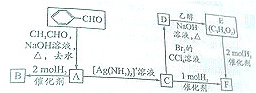
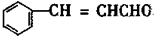 B
B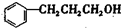 C
C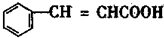 D
D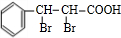
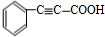 +2H2$→_{△}^{催化剂}$
+2H2$→_{△}^{催化剂}$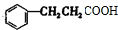 ;加成反应;.
;加成反应;.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
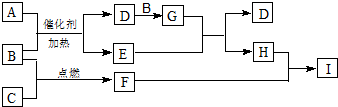
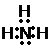 、E的结构式H-O-H、F的化学式为Fe3O4.
、E的结构式H-O-H、F的化学式为Fe3O4.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com