
| A. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | B. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | ||
| C. | H2S+Cl2=S+2HCl | D. | Cu2O+H2SO4=CuSO4+Cu+H2O |
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案科目:高中化学 来源: 题型:选择题
| A. | 分子数 | B. | 压强 | C. | 密度 | D. | 平均摩尔质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
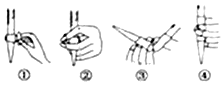
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、纯碱、石膏 | B. | 盐酸、烧碱、小苏打 | ||
| C. | 碳酸、乙醇、硫酸钠 | D. | 磷酸、生石灰、苛性钠 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纯净的液氨中,pN=7 | |
| B. | 纯净的液氨中,c(NH4+)•c(NH2-)>1.0×10-14 | |
| C. | 1 L溶解有0.001 mol NH4C1的液氨溶液,其pN=3 | |
| D. | 1 L溶解有0.001 mol NaNH2的液氨溶液,其pN=11 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-、Fe3+ | B. | HCO3-、Al3+ | C. | Ba2+、SO42- | D. | Na+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com