
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 无色透明溶液中:Ba2+、Fe3+、Cl-、NO3—;
B. 能使酚酞变红的溶液中:Ca2+、K+、HCO3—、CO32—
C. 0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:H+、Al3+、Cl-、NO3—
D. ![]() =10-12的溶液中:NH
=10-12的溶液中:NH![]() 、Cu2+、NO3—、SO42—
、Cu2+、NO3—、SO42—
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某化学课外活动小组拟用铅蓄电池进行电絮凝净水的实验探究,设计的实验装置如图所示,下列叙述正确的是( )

A. Y 的电极反应: Pb-2e- = Pb2+
B. 铅蓄电池工作时SO42-向 Y 极移动
C. 电解池的反应仅有2Al+6H2O![]() 2Al(OH)3+3H2↑
2Al(OH)3+3H2↑
D. 每消耗 103.5 gPb ,理论上电解池阴极上有0.5 molH2生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述不正确的是
A. 化学键的断裂和形成是化学反应中能量变化的根本原因
B. 酸碱中和反应一般是放热反应
C. 等质量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多
D. 因为石墨变成金刚石吸热。所以金刚石比石墨稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学将铁铝合金样品溶解后取样25.00 mL,分离并测定Fe3+的浓度,实验方案设计如下:
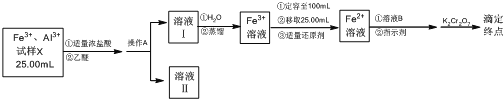
已知:乙醚[(C2H5)2O]是一种易挥发、易燃、有麻醉性的有机化合物,沸点为34.5 ℃,微溶于水。在较高的盐酸浓度下,Fe3+与HCl、乙醚形成化合物[(C2H5)2OH][FeCl4]而溶于乙醚;当盐酸浓度降低时,该化合物解离。
请回答:
(1)操作A的名称是____________。
(2)经操作A后,为判断Fe3+是否有残留,请设计实验方案___________。
(3)滴定前,加入的适量溶液B是________。
A.H2SO3H3PO4 B.H2SO4H3PO4 C.HNO3H3PO4 D.HIH3PO4
(4)滴定达到终点时,消耗0.100 0 mol·L-1 K2Cr2O7溶液6.00 mL。根据该实验数据,试样X中c(Fe3+)为________。
(5)上述测定结果存在一定的误差,为提高该滴定结果的精密度和准确度,可采取的措施是________。
A.稀释被测试样 B.减少被测试样取量
C.增加平行测定次数 D.降低滴定剂浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效消毒剂,可用如下反应制得:2NaClO3+Na2SO3+H2SO4![]() 2ClO2↑+2Na2SO4+H2O,下列说法正确的是( )
2ClO2↑+2Na2SO4+H2O,下列说法正确的是( )
A. 该反应属于复分解反应
B. NaClO3被还原,发生还原反应
C. 反应中Na2SO3作氧化剂
D. 生成6.75 g ClO2时,转移0.2 mol电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于Zn+2HCl=ZnCl2+H2的反应,下列说法正确的是( )
A.单质Zn中Zn的化合价升高,被还原,是氧化剂
B.HCl中H的化合价降低,被氧化,HCl是还原剂
C.H2是还原产物
D.该反应是复分解反应,也是氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(CN)2、(OCN)2等被称为拟卤素,(CN)2在一定条件下氢化可以得到乙二胺(H2NCH2CH2NH2)。回答下列问题:
(1)Fe4[Fe(CN)6]3是较早发现的CN-配合物,其中铁元素呈现两种不同的价态。写出外界离子基态核外电子排布式:________________。
(2)与OCN-互为等电子体的分子为________(填分子式)。
(3)1 mol(CN)2中含有π键的数目为________。
(4)乙二胺中C原子的轨道杂化方式为________。
(5)乙二胺易溶于水,除因为是极性分子外,还可能的原因为________。
(6)含CN-的配合物常用于冶炼黄金。金的晶胞结构如下图所示,晶体中每个Au原子周围紧邻且等距的Au原子有________个。
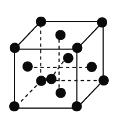
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,反应![]() 达到反应限度的标志是:
达到反应限度的标志是:
A. 正、逆反应速率相等且都等于零
B. c(A2):c(B2):c(AB)= 1:1:2
C. A2、B2和AB的物质的量不再改变
D. 单位时间内消耗n molA2的同时生成2nmolAB
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com