
| A. | 9 mol/L | B. | 4.5 mol/L | C. | 2.5 mol/L | D. | 2.25 mol/L |
分析 根据当加入等体积4mol/L KOH溶液时,生成的沉淀恰好完全溶解,根据反应方程式求出原溶液中铝离子的浓度,根据电荷守恒计算原溶液中钾离子的浓度,再加上所加KOH的中钾离子的物质的量,可计算反应后钾离子的总浓度.
解答 解:设体积均为1L,由于生成沉淀完全溶解,所以反应为
Al3++4OH-=AlO2-+2H2O
1 4
x 4mol
则:x=1mol,即溶液中含有1molAl3+,
原溶液中只含有K+,Al3+和SO42-,根据电荷守恒可得:n(K+)+3n(Al3+)=2n(SO42-),带人n(Al3+)=1mol、n(SO42-)=4mol解得:n(K+)+3×1mol=2×4mol,
解得:n(K+)=5mol,
而反应时又KOH引入了4molK+,所以K+总量为9mol,
反应后溶液体积变为2L,
所以反应后溶液中钾离子浓度为:c(K+)=$\frac{9mol}{2L}$=4.5mol/L,
故选B.
点评 本题考查物质的量浓度的计算,题目难度中等,注意掌握物质的量浓度的概念及计算方法,明确质量守恒和电荷守恒在化学计算中的应用方法.


科目:高中化学 来源: 题型:选择题
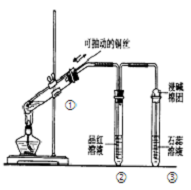
| A. | 装置①能控制反应的发生和结束 | |
| B. | 若将反应后②的试管取下,在通风橱中加热,会产 生刺激性气味的气体,溶液呈红色 | |
| C. | ③中石蕊溶液变红色 | |
| D. | 为确认CuSO4生成,向①中加水,观察溶液颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高二上期中化学试卷(解析版) 题型:实验题
简答下面有关标准氢氧化钠溶液滴定待测盐酸的问题。
(1)盛放待测盐酸的锥形瓶下方垫一张白纸的作用是 。
(2)用酚酞作指示剂,滴定到达终点时,溶液的颜色变化是 。
(3)有下列错误操作:
①碱式滴定管用蒸馏水洗净后,未经标准溶液润洗就注入标准氢氧化钠溶液;
②用酸式滴定管取用待测酸液前,尖嘴部分有气泡,取用过程中气泡消失;
③滴定前,读碱液体积时视线低于碱式滴定管中的液面;滴定后,读出碱液体积时,视线高于碱式滴定管中的液面;
④锥形瓶用待测酸液润洗两次。
哪些错误操作会使盐酸浓度的测定值偏低_____________________。
哪些错误操作会使盐酸浓度的测定值偏高_____________________。
(4)如果用甲基橙代替酚酞作指示剂,此时所得盐酸浓度测定值比用酚酞作指示剂测出的稍大还
是稍小_______________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年黑龙江大庆铁人中学高二上期中化学试卷(解析版) 题型:选择题
下列实验操作能达到测量要求的是( )
A. 用托盘天平称量25.21 g氯化钠
B. 用10 mL量筒量取7.50 mL稀硫酸
C. 用25 mL滴定管量取14.86 mL溶液
D. 用广泛pH试纸测得溶液的pH为4.2
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称取11.70 g食盐 | |
| B. | 用量筒量取12.36 mL盐酸 | |
| C. | 用酸式滴定管量取21.20 mL 0.10 mol•L-1的H2SO4溶液 | |
| D. | 测定溶液的pH时,用洁净、干燥的玻璃棒蘸取溶液,点在用蒸馏水润湿过的pH试纸上,再与标准比色卡比较 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com