
下列各组离子既能与镁粉反应,又能大量共存,且其溶液为无色溶液的是( )
A. Ca2+、Cl﹣、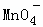 、Na+ B. K+、Cl﹣、
、Na+ B. K+、Cl﹣、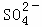 、H+
、H+
C. OH﹣、Na+、Al3+、I﹣ D. H+、Cl﹣、Ba2+、Ag+
考点: 离子共存问题.
分析: A.高锰酸根离子为有色离子,不满足溶液无色的要求;
B.四种离子之间不反应,能够共存,且氢离子能够与镁反应;
C.铝离子与氢氧根离子反应;
D.氯离子与银离子反应生成氯化银沉淀.
解答: 解:A.MnO4﹣为有色离子,不满足溶液无色的条件,故A错误;
B.K+、Cl﹣、H+、SO42﹣之间不反应,能够大量共存,且氢离子能够与镁反应生成氢气,符合要求,故B正确;
C.OH﹣、Al3+之间发生反应,在溶液中不能大量共存,故C错误;
D.Cl﹣、Ag+之间反应生成氯化银沉淀,在溶液中不能大量共存,故D错误;
故选B.
点评: 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN﹣)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH﹣;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4﹣等有色离子的存在.


科目:高中化学 来源: 题型:
在淀粉KI溶液中,滴入少量NaClO溶液,溶液立即变蓝,有关反应的离子方程式是 . 在上述蓝色溶液中,继续滴加足量的NaClO溶液,蓝色逐渐消失,有关反应的离子方程式是 .(提示:碘元素被氧化成IO3﹣)从以上实验可知,ClO﹣、I2、IO3﹣的氧化性由强到弱的顺序是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
国外新近研制的溴化锌蓄电池的基本构造是用碳棒作两极,溴化锌溶液作电解液. 现有四个电极反应:①Zn﹣2e=Zn2+ ②Zn2++2e=Zn ③Br2+2e=2Br﹣ ④2Br﹣﹣2e=Br2.那么,充电时的阳极和放电时的负极反应分别是()
A. ④① B. ②③ C. ③① D. ②④
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的检验说法正确的是( )
A. 将某气体通入品红溶液中,品红溶液褪色,加热后溶液恢复红色,则该气体一定是SO2
B. 钾元素焰色反应的操作:用铂丝蘸取氯化钾置于煤气灯的火焰上进行灼烧,直接观察其焰色
C. NH4+的检验:向待检液中加入NaOH溶液并加热,可生成使湿润的蓝色石蕊试纸变红的气体
D. 待检液加入盐酸可生成使澄清石灰水变浑浊的无色气体,则待检液中一定含有CO32﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
将SO2、H2S、NH3、HCl分别收集于等体积的四个容器中,用导管把四个容器连成一个整体,若使各种气体充分混合(前后条件均相同),混合后容器中的压强与原容器中的压强之比为( )
A. 1:1 B. 1:2 C. 3:4 D. 1:8
查看答案和解析>>
科目:高中化学 来源: 题型:
糖类物质为很多生物生命活动提供能量.
(1)已知 45g葡萄糖在人体内完全氧化为二氧化碳和水,放出701KJ的热量,该反应的热化学方程式 .
(2)以葡萄糖为燃料的微生物燃料电池结构如图所示,其负极反应为: .电池工作过程中溶液中氢离子移动方向从 极区移向 极区(填“正”或“负”)
(3)常温下,用上述电池惰性电极电解100L某浓的硫酸铜溶液,当溶液PH=1时停止电解,则理论上需要葡萄糖的质量为 (假设溶液体积不变)
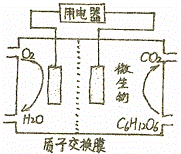
查看答案和解析>>
科目:高中化学 来源: 题型:
已知25℃、101kPa下,石墨、金刚石燃烧的热化学方程式分别为
C(石墨)+O2(g)=CO2(g)△H=﹣393.51kJ•mol﹣1
C(金刚石)+O2(g)=CO2(g)△H=﹣395.41kJ•mol﹣1
据此判断,下列说法中正确的是()
A. 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的低
B. 由石墨制备金刚石是吸热反应;等质量时,石墨的能量比金刚石的高
C. 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的低
D. 由石墨制备金刚石是放热反应;等质量时,石墨的能量比金刚石的高
查看答案和解析>>
科目:高中化学 来源: 题型:
元素的单质及其化合物有着广泛的用途.请根据元素周期表中第三周期元素相关知识回答下列问题.
完成下列填空:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是b.
a.原子半径和简单离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层中p亚层电子数相同的元素名称是硫,磷元素原子最外层电子排布的轨道表示式是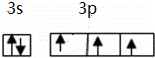 .
.
(3)已知:
化合物 MgO Al2O3 MgCl2 AlCl3
类型 离子化合物 离子化合物 离子化合物 共价化合物
熔点/℃ 2800 2050 714 191
工业制镁时,电解MgCl2而不电解MgO的原因是 ;
制铝时,电解Al2O3而不电解AlCl3的原因是 .
(4)晶体硅(熔点1410℃)是良好的半导体材料.由粗硅制纯硅过程如下:
Si(粗)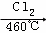 SiCl4
SiCl4 SiCl4(纯)
SiCl4(纯)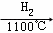 Si(纯)
Si(纯)
在上述由SiCl4制纯硅的反应中,测得每生成1.12kg纯硅需吸收a kJ热量,写出该反应的热化学方程式: .
(5)KClO3可用于实验室制O2,若不加催化剂,400℃时分解只生成两种盐,其中一种是无氧酸盐,另一种盐的阴阳离子个数比为1:1.写出该反应的化学方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com