
分析 根据已知的热化学方程式和盖斯定律,将$\frac{②}{2}-\frac{①}{2}-2③$可得:CH3OH(l)+O2(g)═CO(g)+2H2O(l),△H做相应的变化即可.
解答 解:已知:①2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(g)△H═-akJ•mol-1
②2CO(g)+O2(g)═2CO2(g)△H═-bkJ•mol-1
③H2O(g)═H2O(l)△H═-ckJ•mol-1
根据盖斯定律,将$\frac{②}{2}-\frac{①}{2}-2③$可得:CH3OH(l)+O2(g)═CO(g)+2H2O(l),则△H=$\frac{b-a-4c}{2}$,
故答案为:$\frac{b-a-4c}{2}$.
点评 本题考查学生盖斯定律的应用,是现在考试的热点,难度不大,比较容易.


科目:高中化学 来源: 题型:选择题
| A. | △H2>0 | |
| B. | △H3>△H1 | |
| C. | Mn+SO2═MnO2+S△H=△H2-△H1 | |
| D. | MnO2(s)+SO2(g)═MnSO4(s)△H═△H3-△H2-△H1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用浓硫酸干燥H2、NH3、Cl2等气体 | |
| B. | 向某溶液中加入BaCl2溶液出现白色沉淀,则该溶液中肯定有SO42- | |
| C. | 配制硫酸溶液时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 氨水、铵盐受热都易发生化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

 、C
、C .反应④所用试剂和条件是氢氧化钠醇溶液、加热.
.反应④所用试剂和条件是氢氧化钠醇溶液、加热. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
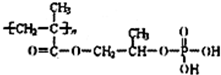
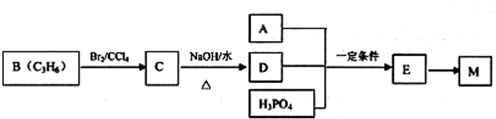
 ,该反应类型是酯化反应.
,该反应类型是酯化反应.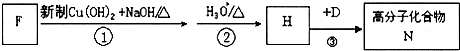
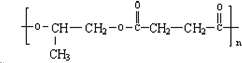
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HBrO3 | B. | XeF2 | C. | HBrO4 | D. | Xe |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com