
氮元素可以形成多种化合物.回答以下问题:
(1)N≡N的键能为942kJ•mol﹣1,N﹣N单键的键能为247kJ•mol﹣1.计算说明N2中的 键更稳定(填“π”或“σ”).
(2)N2与O22+互为等电子体,O22+的电子式可表示为 .
(3)肼(N2H4)分子可视为NH3分子中的一个氢原子被﹣NH2(氨基)取代形成的另一种氮的氢化物.
①NH3分子的空间构型是 ;N2H4分子结构式为 .
②肼可用作火箭燃料,燃烧时发生的反应是:
N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g)△H=﹣1038.7kJ•mol﹣1
若该反应中有4mol N﹣H键断裂,则形成的π键有 mol.
科目:高中化学 来源: 题型:
下列说法错误的是( )。
A.油脂属于酯类物质,能发生水解反应
B.卤代烃在一定条件下能与NaOH水溶液发生反应
C.甲苯能使酸性KMnO4溶液褪色
D.棉花和蚕丝的主要成分都是纤维素
查看答案和解析>>
科目:高中化学 来源: 题型:
一种常用的泡沫灭火器构造如图。内筒a是玻璃瓶,外筒b是钢瓶,平时泡沫灭火器内筒外筒盛有液态试剂,当遇火警时,将灭火器取下倒置,内外筒液体试剂立即混合产生大量CO2泡沫灭火,从液态试剂在灭火器中长久放置和快速灭火两个角度分析,盛放药品正确的是( )
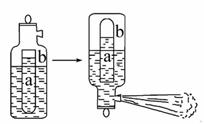
A.a中盛饱和Na2CO3溶液,b中盛Al2(SO4)3溶液
B.a中盛饱和NaHCO3溶液,b中盛Al2(SO4)3溶液
C.a中盛Al2(SO4)3溶液,b中盛饱和Na2C O3溶液
O3溶液
D.a中盛Al2(SO4)3溶液,b中盛饱和NaHCO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各项叙述中,正确的是( )
A.电子层序数越大,s原子轨道的半径越大,形状发生明显的变化
B.在同一电子层上运动的电子,其自旋方向肯定不同
C.电负性的大小可以作为判断金属性和非金属性强弱的尺度
D.原子最外层电子排布是5s1的元素,其氢氧化物不能使氢氧化铝溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
关于键长、键能和键角,下列说法不正确的是 ( )
A.键角的大小与键长、键能的大小无关
B.键长的大小与成键原子的半径和成键数目有关
C.键角是描述分子立体结构的重要参数
D.键能越大,键长越长,共价化合物越稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
取一张用饱和NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圆为白色,外圈呈浅红色。则下列说法错误的是( )
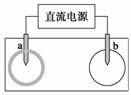
A.b电极是阴极
B.a电极与电源的正极相连接
C.电解过程中,水是氧化剂
D.b电极附近溶液的pH变小
查看答案和解析>>
科目:高中化学 来源: 题型:
电解装置如图所示。图中B装置盛1 L 2 mol·L-1的Na2SO4溶液,A装置中盛1 L 2
mol·L-1 AgNO3溶液。通电后,湿润的淀粉KI试纸的C端变蓝色。电解一段时间后,试回
答:
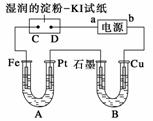
(1)A中发生反应的化学方程式为_________________________________________。
(2)在B中观察到的现象是_____________________________________________。
(3)室温下若从电解开始到时间t时,A、B装置中共收集到0.168 L(标准状况)气体。若电
解过程中无其他副反应发生,且溶液体积变化忽略不计,则在t时,A溶液中酸的浓度为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物Ⅳ为一种重要化工中间体,其合成方法如下:
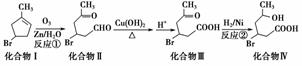
(1)化合物Ⅰ的化学式为________;化合物Ⅳ除了含有—Br还有的官能团是________(填名称)。
(2)化合物Ⅱ具有卤代烃的性质,在一定条件下能生成烯,该反应条件是________。
(3)1 mol化合物Ⅲ与足量NaOH反应消耗NaOH的物质的量为________ mol。
(4)化合物Ⅳ能发生酯化反应生成六元环化合物Ⅴ,写出该反应的化学方程式:__________________________________________。
(5)根据题给化合物转化关系及相关条件,请你推出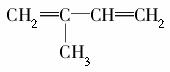 (2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物Ⅵ和Ⅶ,结构简式分别是________、________,它们物质的量之比是________。
(2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物Ⅵ和Ⅶ,结构简式分别是________、________,它们物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“碘钟”实验中,3I-+S2O ===I
===I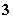 +2SO
+2SO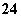 的反应速率可以用I
的反应速率可以用I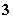 与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
与加入的淀粉溶液显蓝色的时间t来度量,t越小,反应速率越大。某探究性学习小组在20℃进行实验,得到的数据如下表:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| [I-]/mol·L-1 | 0.040 | 0.080 | 0.080 | 0.160 | 0.120 |
| [S2O | 0.040 | 0.040 | 0.080 | 0.020 | 0.040 |
| t/s | 88.0 | 44.0 | 22.0 | 44.0 | t1 |
回答下列问题:
(1) 该实验的目的是______________________________________________________
________________________________________________________________________。
(2)显色时间t1=________。
(3)温度对该反应的反应速率的影响符合一般规律,若在40℃下进行编号③对应浓度的实验,显色时间t2的范围为__________(填字母)。
A.<22.0 s B.22.0~44.0 s
C.>44.0 s D.数据不足,无法判断
(4)通过分析比较上表数据,得到的结论是
________________________________________________________________________
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com