
【题目】碳酸钠是一种重要的化工产品,利用氨碱法生产纯碱的流程如下图所示。

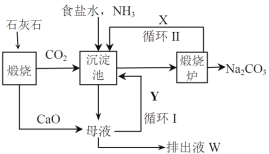
(1)沉淀池中发生反应的化学方程式为___________________;
(2)X是________,Y是_______(填化学式);
(3)排出液W中的溶质除了氢氧化钙外,还有_______、________;(至少两种)
 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:
【题目】某位同学配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是( )
A. 向容量瓶中加水未到刻度线
B. 所用NaOH已经潮解
C. 有少量NaOH溶液残留在烧杯里
D. 用带游码的托盘天平称2.4 g NaOH时误用了“左码右物”方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将足量稀盐酸加到下列固体混合物中,只能发生一种反应的是
A. NaOH、NaCl、NaAlO2 B. KNO3、NaCl、CH3COONa
C. Na2S、(NH4)2SO3、AgNO3 D. Ba(NO3)2、FeSO4、NH4HCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】

现欲用该浓硫酸配制成1mol/L的稀硫酸。现实验室仅需要这种稀硫酸220mL。试回答下列问题:
(1)用量筒量取该浓硫酸 mL;
(2)配制时,必须使用的仪器除量筒、烧杯、玻璃棒外,还缺少的仪器是 ;
(3)配制溶液的过程中,其他操作都正确,下列操作会使所配溶液浓度偏高的是 ;
A.用量筒量取浓硫酸时俯视
B.稀释浓硫酸时,未冷却到室温即转移到容量瓶中
C.量取浓H2SO4后的量筒进行洗涤,并将洗涤液转移到容量瓶中
D.定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至凹液面最低处与刻度线相切
E.容量瓶不干燥
F.定容时,俯视容量瓶刻度线
(4)现需配制0.1mol/LNaOH溶液450mL。
①根据计算得知,所需NaOH的质量为 g;
②配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次) ________。
A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶
B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应m A(g)+n B(g) ![]() p C(g) △H,在密闭容器中进行,下图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线。由曲线分析,下列判断正确的是
p C(g) △H,在密闭容器中进行,下图表示在不同反应时间t 时温度T和压强P与反应物B在混合气体中的百分含量B%的关系曲线。由曲线分析,下列判断正确的是

A. T1<T2,P1>P2,m+n>p,△H<0
B. T1>T2,P1<P2,m+n>p,△H>0
C. T1<T2,P1>P2,m+n<p,△H<0
D. T1>T2,P1<P2,m+n<p,△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分别将一小块钠投入下列溶液中,只有气体放出没有沉淀生成的是( )
A.饱和NaCl溶液 B.稀NaHSO4溶液
C.MgCl2溶液 D.CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】回答下列问题:(均用NA表示阿伏伽德罗常数的值)
(1)0.1molAl2(SO4)3中含有离子总数为 个,Al3+的质量是 ,SO42-的物质的量是 ;
(2)若某原子的摩尔质量是M g /mol,则一个该原子的真实质量是 g;
(3)将标准状况下的aLHCl(g)溶于1000g水中,得到的盐酸密度为bg/mL,则该盐酸的物质的量浓度是 ;
(4)现有14.4g CO和CO2的混合气体,在标准状况下其体积为8.96L;
①该混合气体的平均摩尔质量为 ;
②混合气体中碳原子的个数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g/L)如右图所示。下列叙述正确的是

A.盐酸浓度越大,Ksp(PbCl2)越大
B.PbCl2能与一定浓度的盐酸反应
C.x、y两点对应的溶液中c(Pb2+)相等
D.往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl2(s)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】热激活电池可用作火箭、导弹的工作电源。一种热激活电池的基本结构如图所示,其中作为电解质的无水LiCl-KCl混合物受热熔融后,电池即可瞬间输出电能。该电池总反应为PbSO4+2LiCl+Ca=CaCl2+Li2SO4+Pb。下列有关说法正确的是( )。

A.正极反应式:Ca+2Cl--2e-=CaCl2
B.放电过程中,Li+向负极移动
C.每转移0.1 mol电子,理论上生成20.7 g Pb
D.常温时,在正、负极间接上电流表或检流计,指针不偏转
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com