
【题目】(1)在标准状况下①3.36LNH3②1.204×1023个CH4③18gH2O④0.4molHCl。
a.体积由大到小的顺序_____(填序号,下同)。
b.氢原子个数由大到小的顺序___。
(2)18.6gNa2X含有0.6molNa+,则X2-的摩尔质量为__。
(3)若ag某气体中含有的分子数为b,则cg该气体在标况下体积是(设NA为阿伏加德罗常数的值)____L。
【答案】④>②>①>③ ③>②>①>④ 16g/mol ![]()
【解析】
根据n=N/NA=m/M=V/Vm进行计算,V为标准状况下的气体体积。
(1)在标准状况下①、②、④为气体,③为液体,①3.36LNH3,物质的量为0.15mol,②1.204×1023个CH4的体积为1.204×1023/NA=0.2mol,为4.48L,④0.4molHCl,体积为8.96L,则体积由大到小的顺序为④>②>①>③;①3.36LNH3,物质的量为0.15mol,含有氢原子数目=n(NH3)![]() 3=0.45NA,②1.204×1023个CH4的体积为1.204×1023/NA=0.2mol,含有氢原子数目=n(CH4)
3=0.45NA,②1.204×1023个CH4的体积为1.204×1023/NA=0.2mol,含有氢原子数目=n(CH4)![]() =0.8NA,③18gH2O为1mol,含有氢原子数目=n(H2O)
=0.8NA,③18gH2O为1mol,含有氢原子数目=n(H2O)![]() 2=2NA,④0.4molHCl,含有氢原子数目=n(HCl)
2=2NA,④0.4molHCl,含有氢原子数目=n(HCl)![]() 1=0.4NA,氢原子个数由大到小的顺序为③>②>①>④;
1=0.4NA,氢原子个数由大到小的顺序为③>②>①>④;
(2)0.6molNa+的质量为13.8g,则X的质量为4.8g,已知N(Na+):N(X2-)=2:1,则n(X2-)=0.3mol,M=m/n=4.8g/0.3mol=16g/mol;
(3)cg该气体的分子个数=cg![]() b/ag,则物质的量=c
b/ag,则物质的量=c![]() b/(a
b/(a![]() NA),标况下的体积=c
NA),标况下的体积=c![]() b
b![]() 22.4/(a
22.4/(a![]() NA)L。
NA)L。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】在密闭容器中发生下列反应 aA(g) ![]() cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.7倍,下列叙述正确的是( )
cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,D的浓度为原平衡的1.7倍,下列叙述正确的是( )
A. A的转化率变小 B. 平衡向正反应方向移动
C. D的物质的量变多 D. 再次平衡时的逆反应速率小于原平衡的正反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】区别植物油和矿物油的正确方法是( )
A.加酸性高锰酸钾溶液,振荡
B.加NaOH溶液,煮沸
C.加新制Cu(OH)2悬浊液,煮沸
D.加溴水,振荡
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据元素周期表和元素周期律,判断下列叙述不正确的是

A. 气态氢化物的稳定性:H2O>NH3>SiH4
B. 氢元素与其他元素可形成共价化合物或离子化合物
C. 上图所示实验可证明元素的非金属性:Cl>C>Si
D. 用中文“![]() ”(ào)命名的第118号元素在周期表中位于第七周期0族
”(ào)命名的第118号元素在周期表中位于第七周期0族
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+O2(g)![]() 2SO3(g),△H=-198kJ/mol,在 V2O5存在时反应过程中的能量变化如图所示。下列叙述正确的是
2SO3(g),△H=-198kJ/mol,在 V2O5存在时反应过程中的能量变化如图所示。下列叙述正确的是
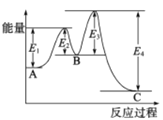
A. △H= E4- E3+E2-E1
B. 加入V2O5后反应经过两步完成,其中第一步决定反应速率
C. 加入V2O5,△H不变,但反应速率改变
D. 向密闭容器中充入2molSO2和1molO2,发生上述反应达平衡时,反应放热198kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于常温下pH=12的稀氨水,下列叙述不正确的是
A. 溶液中c (OH-)=1.010-2 mol·L-1
B. 由水电离出的c (OH-)=1.010-12 mol·L-1
C. 加水稀释后,氨水的电离程度增大
D. 加入少量NH4Cl固体,溶液pH变大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是无机物 A~J在一定条件下的转化关系(部分产物及反应条件未列出)。其中C为红棕色气体;H和I是两种常见的金属单质;过量I与 D溶液反应生成A。
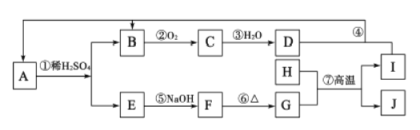
请填写下列空白:
(1)H元素在周期表中的位置是________;写出①的离子反应方程式:_________;检验E溶液中阳离子的最佳试剂为________。
(2)这类反应常用于冶炼高熔点的金属。用MnO2冶炼金属锰的反应中氧化剂与还原剂的物质的量之比为__________。
(3)SCR技术处理机动车尾气时,在催化条件下利用氨气与C反应,生成无污染的物质。发生反应的化学方程式为__________。
(4)F与NaClO、NaOH溶液反应,可制得一种“绿色”高效净水剂K2FeO4。每生成1molFeO42-时转移____________mol电子。
(5)B为大气污染物,利用炭粉可以将其还原为无污染的物质X2。
已知:X2(g)+O2(g)=2XO(g) △H=+180.6kJ/mol
C(s)+O2(g)=CO2(g) △H=-393.5kJ/mol
写出用碳粉还原B的热化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机化合物的结构简式如图所示.有关该化合物的叙述不正确的是( )

A. 该有机物的分子式为C11H12O2
B. 1mol该物质最多能与4mol H2发生加成反应
C. 该有机物在一定条件下,可以发生取代、氧化、酯化反应
D. 该有机物能与热的新制氢氧化铜悬浊液反应,生成砖红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是
A. 铅蓄电池在放电过程中,负极质量减小,正极质量增加
B. 常温下,反应C(s)+CO2(g)===2CO(g)不能自发进行,则该反应的![]()
C. 应用盖斯定律可计算某些难以直接测量的反应焓变
D. 1g碳与适量水蒸气反应生成 CO和H2,吸收10.94kJ热量,则热化学方程式为:C(s)+H2O(g)═CO(g)+H2(g)△H=+131.28kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com