
| A. | C3H8 | B. | C2H6O | C. | C4H8O | D. | C4H8O2 |
分析 根据物质的组成判断耗氧量,物质的量相同的烃CxHy的耗氧量取决于x+$\frac{y}{4}$,物质的量相同的含烃氧衍生物CxHyOz耗氧量取决于x+$\frac{y}{4}$-$\frac{z}{2}$,据此判断物质的量相同各物质的耗氧量.
解答 解:A、C3H8,其x+$\frac{y}{4}$=3+$\frac{8}{4}$=5,即1molC3H8消耗5mol氧气;
B、C2H6O,其于x+$\frac{y}{4}$-$\frac{z}{2}$=2+$\frac{6}{4}$-$\frac{1}{2}$=4,即1molC2H6O消耗4mol氧气;
C、C4H8O的消耗氧气的量等于C4H6消耗氧气的量,其x+$\frac{y}{4}$=4+$\frac{6}{4}$=6.5,即1molC4H8O消耗6.5mol氧气;
D、C4H8O2的消耗氧气的量为x+$\frac{y}{4}$-$\frac{z}{2}$=4+2-1=5,即1molC4H8O2消耗5mol氧气;
故耗氧量最大的是C4H8O.
故选:C.
点评 考查有机物耗氧量规律,难度较小,掌握有机物耗氧量规律,注意知识的归纳总结.


科目:高中化学 来源: 题型:解答题

 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
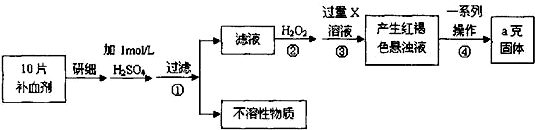
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.04 mol/(L•s) | B. | 0.12 mol/(L•s) | C. | 0.4 mol/(L•s) | D. | 1.2 mol/(L•s) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “辽宁舰”上用于舰载机降落拦阻索的特种钢缆,属于新型无机非金属材料 | |
| B. | 氧氧化铁溶胶、含塑化剂的白酒、含有细菌的矿泉水均具有丁达尔效应 | |
| C. | 对“地沟油”蒸馏可以获得汽油 | |
| D. | 用K2FeO4代替Cl2处理饮用水,既有杀菌消毒作用,又有净水作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PVC保鲜膜属于链状聚合物,在加热时易熔化,能溶于氯仿 | |
| B. | 汽车尾气排放的NO2等气体是造成光化学污染的主要原因 | |
| C. | 点燃爆竹后,硫燃烧生成SO3 | |
| D. | 误食含有大量Cu2+的食物可以服用鲜牛奶解毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 强电解质都是离子化合物,因此NaCl是离子化合物 | |
| B. | 亚硫酸溶液的导电能力可能比稀硫酸强 | |
| C. | SO3溶于水,其水溶液能导电,SO3是电解质 | |
| D. | 石墨是单质,能导电,因此石墨是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
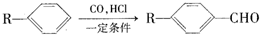 为合成某种液晶材料的中间体M,有人提出如下不同的合成路径:
为合成某种液晶材料的中间体M,有人提出如下不同的合成路径: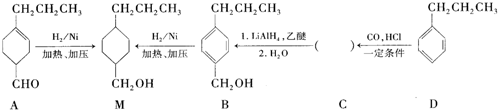
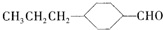 和
和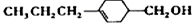 (写结构简式)生成.
(写结构简式)生成.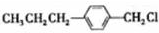 .
.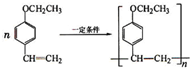 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com