
【题目】某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图Ⅰ-Ⅳ所示。
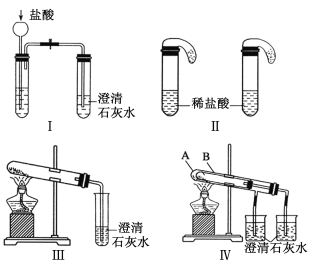
(1)只根据图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)___________;
(2)图Ⅲ、Ⅳ所示实验均能鉴别这两种物质,其反应的化学方程式为___________;
与实验Ⅲ相比,实验Ⅳ的优点是(填选项序号)_____;
A.Ⅳ比Ⅲ复杂 B.Ⅳ比Ⅲ安全
C.Ⅳ比Ⅲ操作简便 D.Ⅳ可以做到一套装置同时进行两个对比实验,而Ⅲ不能
(3)若用实验装置Ⅳ验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的固体最好是______;
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应,
①当石灰水过量时,其离子方程式是_____________;
②当碳酸氢钠与氢氧化钙物质的量之比为2:1时,所得溶液中溶质的化学式为______,请设计实验检验所得溶液中溶质的阴离子__________。
【答案】Ⅱ 2NaHCO3![]() Na2CO3+H2O+CO2↑,CO2+Ca(OH)2=CaCO3↓+H2O D NaHCO3 HCO3-+Ca2++OH-=CaCO3↓+H2O Na2CO3 取少量上层清液于试管中,加入适量氯化钙溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO32-
Na2CO3+H2O+CO2↑,CO2+Ca(OH)2=CaCO3↓+H2O D NaHCO3 HCO3-+Ca2++OH-=CaCO3↓+H2O Na2CO3 取少量上层清液于试管中,加入适量氯化钙溶液,振荡,若有白色沉淀生成,则证明溶液中含有CO32-
【解析】
(1)碳酸钠和盐酸反应分两步进行,盐酸和碳酸钠、碳酸氢钠反应都生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊;
(2)碳酸氢钠在加热条件下能分解生成碳酸钠和水、二氧化碳;根据两个实验的区别分析;
(3)不直接加热碳酸氢钠就能分解更说明碳酸氢钠不稳定;
(4)①碳酸氢钠和氢氧化钙发生复分解反应;
②当碳酸氢钠过量时,碳酸氢钠和氢氧化钙反应生成碳酸钠、碳酸钙和水,碳酸钠和和氯化钙反应生成白色碳酸钙沉淀,据此设计实验。
(1)Na2CO3和NaHCO3均能与盐酸反应生成使澄清石灰水变浑浊的CO2,故实验Ⅰ不能鉴别Na2CO3和NaHCO3。实验Ⅱ中,盐酸和碳酸氢钠反应立即产生气泡,盐酸和碳酸钠先反应生成碳酸氢钠,无明显现象,当所有的碳酸钠完全转化为碳酸氢钠后,碳酸氢钠和盐酸反应生成二氧化碳气体,所以看到的现象不同,故II能鉴别碳酸钠和碳酸氢钠两种白色固体物质;
(2)NaHCO3受热分解:2NaHCO3![]() Na2CO3+H2O+CO2↑,反应产生的CO2能够使澄清的石灰水变浑浊,反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O ;Na2CO3受热不分解。与实验Ⅲ相比,实验Ⅳ的优点是一套装置可以同时进行两个对比实验。
Na2CO3+H2O+CO2↑,反应产生的CO2能够使澄清的石灰水变浑浊,反应方程式为:CO2+Ca(OH)2=CaCO3↓+H2O ;Na2CO3受热不分解。与实验Ⅲ相比,实验Ⅳ的优点是一套装置可以同时进行两个对比实验。
(3)从实验Ⅳ可以看出,A中温度高,B中温度低,若A中装Na2CO3,B中装NaHCO3,在这种情况下,与B相连试管中的澄清石灰水变浑浊,而与A相连试管中的澄清石灰水不变浑浊,更能说明NaHCO3比Na2CO3易分解;
(4)碳酸氢钠与氢氧化钙反应时,反应物的量相对不同,生成物不同,若澄清石灰水过量,反应为Ca(OH)2+NaHCO3=CaCO3↓+NaOH+H2O;当碳酸氢钠与氢氧化钙物质的量之比为2:1时,反应为2NaHCO3+Ca(OH)2=CaCO3↓+Na2CO3+2H2O,所得溶液中溶质为Na2CO3。检验所得溶液中溶质的阴离子CO32-的方法:取少量上层清液于试管中,加入适量氯化钙溶液,振荡,若有白色沉淀生成,即可证明溶液中含有CO32-。


科目:高中化学 来源: 题型:
【题目】已知同温、同浓度时,酸性:H2SO3>H2CO3>HSO3- >HCO3-
【1】用方程式表示NaHSO3溶液中存在的三个平衡体系(不考虑亚硫酸的分解):
①_________、②_________、③_________。
【2】0.1 mol L-1 的 NaHSO3溶液中离子浓度:c(SO32-)______c(HSO3-)(填 “>”、“<”或“=”);要使其中的c(H+)和c(SO32-)都减小,可行的方法是________________。
A 加入过量CaO(s) B 加入少量NaOH(s) C 通入过量HCl(g) D 加入少量的H2O2(aq)
【3】0.1mol L的Na2SO3溶液呈____性(填“酸”、“碱”或“中”),其电荷守恒式: c(Na+)+c(H+)=_______。
【4】H2SO3和NaHCO3溶液的离子方程式为:___________。
【5】NaHSO3溶液在不同温度下均可被过量KIO3酸性溶液氧化,当NaHSO3完全消耗即I2有析出,写出该反应的离子方程式:___________。
【6】将NaHSO3(含少量淀粉)和酸性溶液KIO3(过量)混合,记录10-50℃间溶液变蓝时间,实验結果见下图。请描述曲线变化的规律________。
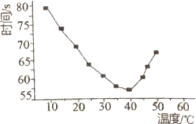
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如图所示装置进行实验,将液体A逐滴加入到固体B中,下列叙述不正确的是
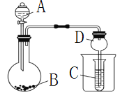
A. 若A为浓硫酸,B为K2SO3,C中盛品红溶液,则C中溶液褪色
B. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中先变浑浊后澄清
C. 若A为醋酸,B为CaCO3,C中盛Na2SiO3溶液,则C中溶液中变浑浊
D. 若A为双氧水,B为MnO2,C中盛Na2S溶液,则C中溶液中变浑浊
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将高碘酸H5IO6加入MnSO4溶液中可使溶液呈紫红色,已知H5IO6在反应中发生如下过程:H5IO6→HIO3。完成下列填空:
(1)将该反应的氧化剂、还原剂及配平后的系数填入正确位置,并用单线桥法标明电子转移的方向和数目。________________
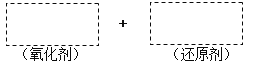
(2)生成2 mol的HIO3转移的电子数为___________
(3)若向H5IO6溶液中加入足量的下列物质,能将碘元素还原成I的是_____(选填序号)
a.盐酸 b.硫化氢 c.溴化钠 d.硫酸亚铁
(4)若向H5IO6的溶液中加入过量的过氧化氢溶液,再加入淀粉溶液,溶液变蓝,同时有大量气体产生。请写出此反应的化学方程式:___________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组设计实验探究CuSO4分解产物
Ⅰ.甲同学选择下列装置设计实验探究硫酸铜分解的气态产物SO3、SO2和O2,并验证SO2的还原性。
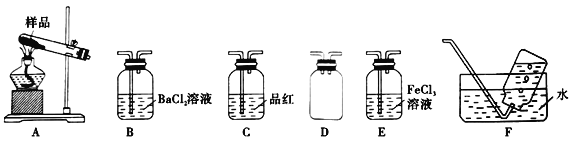
回答下列有关问题:
(1)上述装置按气流从左至右排序为A、D、___E、F(填代号)。
(2)装置D的作用是____;能证明有SO3生成的实验现象是____。
(3)在实验过程中C装置中红色溶液逐渐变为无色溶液,说明A中分解产物有:___;待C中有明显现象后,F开始收集气体,F装置中集气瓶收集到了少量气体,该气体是___(填化学式)。
(4)为了验证SO2的还原性,取E装置中反应后的溶液于试管中,设计如下实验:
a.滴加少量的NH4SCN溶液 b.滴加少量的K3[Fe(CN)6]溶液
c.滴加酸性KMnO4溶液 d.滴加盐酸酸化的BaCl2溶液
其中,方案合理的有____(填代号),写出E装置中可能发生反应的离子方程式:___。
Ⅱ.乙同学利用A中残留固体验证固体产物(假设硫酸铜已完全分解)查阅资料知,铜有+2、+1价,且分解产物中不含0价的铜。Cu2O在酸性条件下不稳定,发生反应:Cu2O+2H+ =Cu+Cu2++H2O。
(5)为了验证固体产物中是否有Cu2O,设计了下列4种方案,其中能达到实验目的的是____。
甲:取少量残留固体于试管,滴加足量的稀硝酸,观察溶液颜色是否变为蓝色
乙:取少量残留固体于试管,滴加足量的稀硫酸,观察溶液颜色是否变为蓝色
丙:取少量残留固体于试管,滴加足量的稀盐酸,观察是否有红色固体生成
丁:取少量残留固体于试管,通入氢气,加热,观察是否生成红色固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表隐含着许多信息和规律。以下所涉及的元素均为中学化学中常见的短周期元素,其原子半径及主要化合价列表如下,其中R2Q2用于呼吸面具或潜水艇中作为氧气来源。

下列说法正确的是
A. T、Z的最高价氧化物对应水化物的酸性T<Z
B. R、X、Y的单质失去电子能力最强的是X
C. M与Q形成的是离子化合物
D. M、Q、Z都在第2周期
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
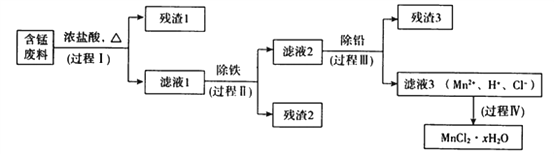
资料a.Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b.生成氢氧化物沉淀的pH
Mn(OH)2 | Pb(OH)2 | Fe(OH)3 | |
开始沉淀时 | 8.1 | 6.5 | 1.9 |
完全沉淀时 | 10.1 | 8.5 | 3.2 |
注:金属离子的起始浓度为0.1 mol·L-1
(1)过程Ⅰ的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnOOH与浓盐酸反应的离子方程式是_______________________________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:_________________________________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:
a.2Fe2++Cl2=2Fe3+2Cl-
b.4Fe2++O2+4H+=2Fe3++2H2O
c.……
写出c的离子方程式:____________________。
(2)过程Ⅱ的目的是除铁。有如下两种方法,
ⅰ.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ⅱ.焙烧法:将滤液1浓缩得到的固体于290℃焙烧,冷却,取焙烧物,加水溶解,过滤,再加盐酸酸化至pH小于5.5。
已知:焙烧中发生的主要反应为2FeCl3+3O2=2Fe2O3+3Cl2,MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH应控制在_____________之间。
②两种方法比较,氨水法除铁的缺点是____________。
(3)过程Ⅲ的目的是除铅。加入的试剂是____________。
(4)过程Ⅳ所得固体中的x的测定如下,取m1g样品,置于氯化氢氛围中加热至失去全部结晶水时,质量变为m2g。则x=____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,2H2(g)+O2(g)![]() 2H2O(l)+566kJ。下列说法错误的是
2H2O(l)+566kJ。下列说法错误的是
A.H2![]() H+H的过程需要吸热
H+H的过程需要吸热
B.若生成2mol水蒸气,则放出的热量大于566kJ
C.2g氢气完全燃烧生成液态水所释放的能量为283kJ
D.2mol氢气与1mol氧气的能量之和大于2mol液态水的能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加碘食盐是含KIO3的食盐,其中KIO3可由反应KI+3Cl2+3H2O=KIO3+6HCl制取。市面上销售的加碘食盐中的碘元素含量为20~50mg/kg。请计算:制取1000kg含碘元素25.4mg/kg的加碘食盐,需要消耗Cl2的体积是多少___?(标准状况)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com