
| A£® | HCl”śCl2”śHClO”śNaClO | B£® | Na”śNa2O2”śNa2CO3”śNaHCO3 | ||
| C£® | Mg”śMgO”śMg£ØOH£©2”śMgCl2 | D£® | Na”śNaOH”śNaHCO3”śNa2CO3 |
·ÖĪö A”¢ÅØŃĪĖįÓėĒæŃõ»Æ¼ĮČē¶žŃõ»ÆĆĢ”¢øßĆĢĖį¼Ų”¢ĀČĖį¼ŲµČ·“Ӧɜ³ÉĀČĘų£¬ĀČĘųÓėĖ®·“Ӧɜ³É“ĪĀČĖį£¬“ĪĀČĖįŹĒČõĖį£¬Óė¼ī·“Ӧɜ³ÉŃĪ£»
B”¢ÄĘŌŚŃõĘųÖŠČ¼ÉÕ²śĪļÉś³É¹żŃõ»ÆÄĘ£¬¹żŃõ»ÆÄĘŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįÄĘŗĶŃõĘų£¬Ģ¼ĖįÄĘæÉŅŌÓė¶žŃõ»ÆĢ¼”¢Ė®·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ£»
C”¢Ć¾ŗĶŃõĘų·“Ӧɜ³ÉŃõ»ÆĆ¾£¬Ńõ»ÆĆ¾²»ÄÜŅ»²½×Ŗ»ÆĪŖĒāŃõ»ÆĆ¾£»
D”¢ÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘ£¬ĒāŃõ»ÆÄĘŗĶ¹żĮ涞Ńõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ£¬Ģ¼ĖįĒāÄĘŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĢ¼ĖįÄĘ£®
½ā“š ½ā£ŗA”¢ÅØŃĪĖįÓėĒæŃõ»Æ¼ĮČē¶žŃõ»ÆĆĢ”¢øßĆĢĖį¼Ų”¢ĀČĖį¼ŲµČ·“Ӧɜ³ÉĀČĘų£¬ĀČĘųÓėĖ®·“Ӧɜ³É“ĪĀČĖį£¬“ĪĀČĖįŹĒČõĖį£¬ÓėĒāŃõ»ÆÄĘ·“Ӧɜ³É“ĪĀČĖįÄĘÓėĖ®£¬¹ŹAÕżČ·£»
B”¢ÄĘŌŚŃõĘųÖŠČ¼ÉÕ²śĪļÉś³É¹żŃõ»ÆÄĘ£¬¹żŃõ»ÆÄĘŗĶ¶žŃõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįÄĘŗĶŃõĘų£¬Ģ¼ĖįÄĘæÉŅŌÓė¶žŃõ»ÆĢ¼”¢Ė®·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ£¬¹ŹBÕżČ·£»
C”¢Ć¾ŗĶŃõĘų·“Ӧɜ³ÉŃõ»ÆĆ¾£¬Ńõ»ÆĆ¾²»ÄÜŅ»²½×Ŗ»ÆĪŖĒāŃõ»ÆĆ¾£¬¹ŹC“ķĪó£»
D”¢ÄĘŗĶĖ®·“Ӧɜ³ÉĒāŃõ»ÆÄĘ£¬ĒāŃõ»ÆÄĘŗĶ¹żĮ涞Ńõ»ÆĢ¼·“Ӧɜ³ÉĢ¼ĖįĒāÄĘ£¬Ģ¼ĖįĒāÄĘŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉĢ¼ĖįÄĘ£¬æÉŅŌŹµĻÖ×Ŗ»Æ£¬¹ŹDÕżČ·£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²éŌŖĖŲ»ÆŗĻĪļĪļÖŹÖ®¼äµÄ×Ŗ»ÆµČ£¬±Č½Ļ»ł“”£¬ÕĘĪÕĪļÖŹµÄŠŌÖŹŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬×¢Ņā»ł“”ÖŖŹ¶µÄ»żĄŪÕĘĪÕ£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 ŅŃÖŖ»Æѧ·“Ó¦N2+3H22NH3µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ
ŅŃÖŖ»Æѧ·“Ó¦N2+3H22NH3µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Cu2+”¢SO32-”¢OH- | B£® | Na+”¢H+”¢SO42- | C£® | OH-”¢Fe2+”¢SO42- | D£® | Na+”¢H+”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
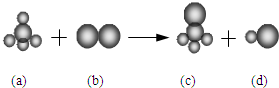 ŅŃÖŖÓÉČżÖÖŌŖĖŲ¹¹³ÉµÄĖÄÖÖĪļÖŹ“ęŌŚĻĀĮŠ·“Ó¦£¬ĘäÖŠaµÄ·Ö×Óæռ乹ŠĶĪŖÕżĖÄĆęĢ壮×é³Éa·Ö×ÓµÄĮ½ÖÖŌŖĖŲµÄŌ×ÓŠņŹżŗĶŠ”ÓŚ10£¬×é³Éb·Ö×ÓµÄŌŖĖŲĪŖµŚČżÖÜĘŚµÄŌŖĖŲ£®ŌņĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©
ŅŃÖŖÓÉČżÖÖŌŖĖŲ¹¹³ÉµÄĖÄÖÖĪļÖŹ“ęŌŚĻĀĮŠ·“Ó¦£¬ĘäÖŠaµÄ·Ö×Óæռ乹ŠĶĪŖÕżĖÄĆęĢ壮×é³Éa·Ö×ÓµÄĮ½ÖÖŌŖĖŲµÄŌ×ÓŠņŹżŗĶŠ”ÓŚ10£¬×é³Éb·Ö×ÓµÄŌŖĖŲĪŖµŚČżÖÜĘŚµÄŌŖĖŲ£®ŌņĻĀĮŠÅŠ¶ĻÕżČ·µÄŹĒ£Ø””””£©| A£® | ĖÄÖÖ·Ö×ÓÖŠµÄ»Æѧ¼ü¾łŹĒ¼«ŠŌ¼ü | B£® | a”¢c·Ö×ÓÖŠÖŠŠÄŌ×Ó¾łĪŖsp3ŌÓ»Æ | ||
| C£® | ĖÄÖÖ·Ö×ÓÖŠ¼ČÓŠ¦Ņ¼ü£¬ÓÖÓŠ¦Š¼ü | D£® | b”¢d·Ö×ÓÖŠ¹²¼Ū¼üµÄ¼üÄÜb“óÓŚd |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ĒāŃõ»ÆÄĘČÜŅŗ | B£® | ĒāŃõ»ÆĶŠü×ĒŅŗ | C£® | ŹÆČļŹŌŅŗ | D£® | Ģ¼ĖįÄĘČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
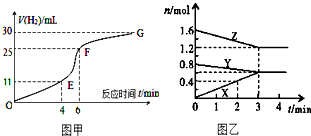 »Æѧ·“Ó¦ĖŁĀŹŗĶĻŽ¶ČŹĒ֊ѧ»ÆѧŌĄķÖŠŗÜÖŲŅŖ²æ·Ö£¬øł¾ŻĖłŃ§ÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā£ŗ
»Æѧ·“Ó¦ĖŁĀŹŗĶĻŽ¶ČŹĒ֊ѧ»ÆѧŌĄķÖŠŗÜÖŲŅŖ²æ·Ö£¬øł¾ŻĖłŃ§ÖŖŹ¶»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆ“×Ėį³żĖ®¹ø£ŗCaCO3+2H+ØTCa2++CO2”ü+H2O | |
| B£® | ĀČŅŅĖįÓėĒāŃõ»ÆÄĘČÜŅŗ¹²ČČ£ŗCH2ClCOOH+OH-$\stackrel{”÷}{”ś}$CH2ClCOO-+H2O | |
| C£® | ÓĆŠĀÖĘĒāŃõ»ÆĶŠü×ĒŅŗ¼ģŃéŅŅČ©ÖŠµÄČ©»ł£ŗCH3CHO+2Cu£ØOH£©2$\stackrel{”÷}{”ś}$CH3COOH+Cu2O”ż+2H2O | |
| D£® | ±½·ÓÄĘČÜŅŗÖŠĶØČėÉŁĮ涞Ńõ»ÆĮņ£ŗC6H5O-+SO2+H2O”śC6H5OH+HSO3- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com