


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源:不详 题型:填空题
| ① |
| ② |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.镁片与铝片的形状和大小 |
| B.盐酸的浓度 |
| C.盐酸的体积 |
| D.产生气体的体积 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.液态金属铅中含有离子健 | B.20.7g铅与足量稀盐酸反应生成2.24L氢气 |
| C.可溶性铅盐会引起中毒 | D.液态金属铅是由于其中的氢键作用而形成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

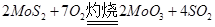 ,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为________。
,该反应的还原剂是__________。当有1mol MoS2反应时,还原剂失去电子的物质的量为________。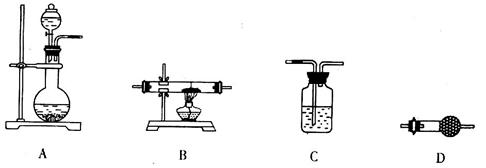
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 盐酸反应)、
盐酸反应)、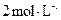 盐酸、5%NaOH溶液、饱和
盐酸、5%NaOH溶液、饱和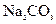 溶液、饱和
溶液、饱和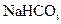 溶液和蒸馏水。
溶液和蒸馏水。
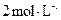 盐酸,塞紧塞子。在B、E中均加入饱和
盐酸,塞紧塞子。在B、E中均加入饱和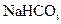 溶液,如图所示,记下量气管读数。
溶液,如图所示,记下量气管读数。 面在同一水平面上,最后读数时右管的液面高于左管的液面,应进行的操作是
面在同一水平面上,最后读数时右管的液面高于左管的液面,应进行的操作是  。
。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
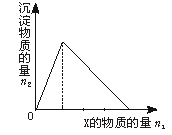
| | A | B | C | D |
| X | NaOH | AlCl3 | HCl | Na[Al (OH)4] |
| Y | AlCl3 | NaOH | Na[Al (OH)4] | HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com