
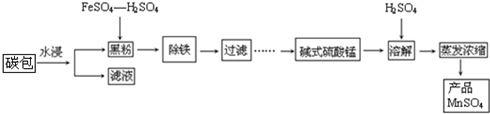
·ÖĪö £Ø1£©³żĮĖCa£ØOH£©2ŗĶNaClĶā£¬ĘäĖūµÄ¹ĢĢåĪļÖŹ£¬¾łŹĒÉżøßĪĀ¶Č£¬Čܽā¶ČŌö“󣬻ņŹĒ½Į°čŅ²ÄܼÓæģČܽā£¬»ņÕߏĒĢįøßĮņĖįµÄÅØ¶ČµČ£»
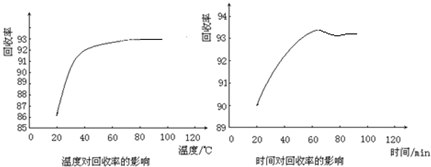
£Ø2£©“ÓĶ¼ĻóæÉŅŌ擳ö£¬“Ó80”ęæŖŹ¼£¬»ŲŹÕĀŹ“ļµ½×īøßÖµ²¢¼øŗõ²»ŌŁÉżøߣ¬“ĖŹ±Ó¦“ÓŗÄÄܵĽĒ¶ČĄ“æ¼ĀĒ£»ŌŚ60”ꏱ£¬»ŲŹÕĀŹ“ļµ½×īøßÖµ£»
£Ø3£©¢ŁMnO2ÖŠµĪČėKIŗó£¬ŌŚĖįŠŌ»·¾³ĻĀ£¬MnO2°ŃI-Ńõ»ÆĪŖI2£¬MnO2±»»¹ŌĪŖMn2+£¬¾Ż“ĖŠ“³öĄė×Ó·½³ĢŹ½£»
¢ŚĻė²½ÖčbĖłµĆµÄŗ¬I2µÄČÜŅŗÖŠµĪ¼Ó1mL0.5%µķ·ŪČÜ£¬ČÜŅŗ±äĄ¶£»²½ÖčCÖŠ£¬ÓĆÓĆcmol/LµÄNa2S2O3ČÜŅŗĄ“µĪ¶ØÉś³ÉµÄI2£¬µ±Ą¶É«±äĪŽÉ«Ź±£¬“ļµĪ¶ØÖÕµć£»
¢ŪÓÉ·“Ó¦æÉÖŖ£ŗ4MnO2 ”«4I2 ”«Na2S2O3 £¬øł¾ŻĻūŗĵÄNa2S2O3µÄĪļÖŹµÄĮ棬Ēó³öMnO2µÄĪļÖŹµÄĮ棬“Ó¶ųĒó³öĢ¼°üÖŠMnO2µÄÖŹĮæ·ÖŹż£®
½ā“š ½ā£ŗ£Ø1£©³żĮĖCa£ØOH£©2ŗĶNaClĶā£¬ĘäĖūµÄ¹ĢĢåĪļÖŹ£¬¾łŹĒÉżøßĪĀ¶Č£¬Čܽā¶ČŌö“ó£¬ĪŖĮĖ¼Óæģ¼īŹ½ĮņĖįĆĢµÄČܽāĖŁĀŹ£¬æɲÉČ”µÄ“ėŹ©ÓŠ¼ÓČČ£¬»ņŹĒ½Į°čŅ²ÄܼÓæģČܽā£¬»ņÕߏĒĢįøßĮņĖįµÄÅØ¶ČµČ£¬
¹Ź“š°øĪŖ£ŗ¼ÓČČ”¢½Į°č”¢ŹŹµ±ĢįøßĮņĖįµÄÅØ¶ČµČ£»
£Ø2£©“ÓĶ¼ĻóæÉŅŌ擳ö£¬“Ó80”ęæŖŹ¼£¬»ŲŹÕĀŹ“ļµ½×īøßÖµ²¢¼øŗõ²»ŌŁÉżøߣ¬¶ųĪĀ¶ČŌ½øߣ¬ŗÄÄÜŌ½¶ą£¬“ÓŗÄÄܵĽĒ¶ČĄ“æ¼ĀĒ£¬Ó¦Ń”¶ØµÄŹŹŅĖĪĀ¶ČŹĒ80”ę£»ŌŚ60”ꏱ£¬»ŲŹÕĀŹ“ļµ½×īøßÖµ£¬Ź±¼äŃÓŗóŗ󣬻ŲŹÕĀŹ·“¶ųĻĀ½µ£¬¹ŹŹŹŅĖµÄ·“Ó¦Ź±¼äĪŖ60min£¬¹Ź“š°øĪŖ£ŗ80”ę£¬60min£»
£Ø3£©¢ŁMnO2ÖŠµĪČėKIŗó£¬ŌŚĖįŠŌ»·¾³ĻĀ£¬MnO2°ŃI-Ńõ»ÆĪŖI2£¬MnO2±»»¹ŌĪŖMn2+£¬¹ŹĄė×Ó·½³ĢŹ½ĪŖ£ŗMnO2+I-+H+=Mn2++I2+2H2O£¬
¹Ź“š°øĪŖ£ŗMnO2+I-+H+=Mn2++I2+2H2O£»
¢ŚĻė²½ÖčbĖłµĆµÄŗ¬I2µÄČÜŅŗÖŠµĪ¼Ó1mL0.5%µķ·ŪČÜ£¬ČÜŅŗ±äĄ¶£»²½ÖčCÖŠ£¬ÓĆcmol/LµÄNa2S2O3ČÜŅŗĄ“µĪ¶ØÉś³ÉµÄI2£¬¹Ź“ļµĪ¶ØÖÕµćŹ±£¬Ą¶É«±äĪŽÉ«ĒŅ°ė·ÖÖÓ²»»Öø“ŌÉ«¼““ļµĪ¶ØÖÕµć£¬
¹Ź“š°øĪŖ£ŗČÜŅŗÓÉĄ¶É«±äĪŖĪŽÉ«ĒŅ°ė·ÖÖÓ²»»Öø“ŌÉ«£»
¢ŪµĪ¶Ø¹ż³ĢÖŠĻūŗĵÄNa2S2O3µÄĪļÖŹµÄĮæn=CV=cmol/L”ĮV”Į10-3L=10-3CVmol£¬ÉčMnO2µÄĪļÖŹµÄĮæĪŖXmol£¬
¾Ż·“Ó¦æÉÖŖ£ŗ4MnO2 ”«4I2 ”«Na2S2O3
4 1
Xmol 10-3CVmol
æÉµĆ£ŗ$\frac{4}{X}$=$\frac{1}{10{\;}^{-3}CV}$
½āµĆX=4”Į10-3CVmol
¹ŹMnO2µÄÖŹĮæm=nM=4”Į10-3CVmol”Į87g/mol=0.348CVg
¹ŹĢ¼°üÖŠMnO2µÄÖŹĮæ·ÖŹż=$\frac{0.348CVg}{0.500g}$”Į100%=69.6Cv%
¹Ź“š°øĪŖ£ŗ69.6Cv%£®
µćĘĄ ±¾Ģāæ¼²éĮĖµĪ¶Ø¹ż³ĢÖŠµÄÓŠ¹Ų¼ĘĖćŗĶŹµŃé²Ł×÷ŅŌ¼°Ńõ»Æ»¹Ō·“Ó¦µÄŹéŠ“£¬øł¾ŻµĪ¶ØĪļÖŹÖ®¼äµÄ¼ĘĮæ¹ŲĻµĄ“½ųŠŠ¼ĘĖć£¬×ŪŗĻŠŌ½ĻĒ棬µ«ÄŃ¶Č²»“ó£®


 ĆūŠ£æĪĢĆĻµĮŠ“š°ø
ĆūŠ£æĪĢĆĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÓĆĖ«ŃõĖ®“śĢęøßĆĢĖį¼ŲÖĘŃõĘų | |
| B£® | ÓƶąĮæµÄĀČĘų½ųŠŠŠŌÖŹŹµŃé | |
| C£® | ÓĆäåĖ®“śĢęµāĖ®½ųŠŠŻĶČ”ŹµŃé | |
| D£® | ÓĆĶ·Ū“śĢęĶĖæ½ųŠŠĶŗĶÅØĻõĖįµÄ·“Ó¦ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuÓėĻõĖį | B£® | ³ĪĒåµÄŹÆ»ŅĖ®ÓėCO2 | ||
| C£® | NaÓėO2 | D£® | AlCl3Óė°±Ė® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ×éŗĻŠņŗÅ | ¢ń | ¢ņ | ¢ó | ¢ō | ¢õ | ¢ö |
| ×éŗĻŹż¾Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| ĪĀ¶Č | 283K | 293K | 303K |
| Čܽā¶Č£Øg/100g H2O£© | 2.5 | 3.9 | 5.6 |
| ŹµŃé²½Öč | Ō¤ĘŚĻÖĻóŗĶ½įĀŪ |
| ²½Öč1£ŗČ”ŹŹĮæŹŌ¼ĮÓŚ½ą¾»ÉÕ±ÖŠ£¬¼ÓČė×ćĮæÕōĮóĖ®£¬³ä·Ö½Į°č£¬¾²ÖĆ£¬¹żĀĖ£¬µĆĀĖŅŗŗĶ³Įµķ£® | |
| ²½Öč2£ŗČ”ŹŹĮæĀĖŅŗÓŚŹŌ¹ÜÖŠ£¬µĪ¼ÓĻ”ĮņĖį£® | ³öĻÖ°×É«³Įµķ£¬ĖµĆ÷øĆŹŌ¼ĮÖŠÓŠBa2+“ęŌŚ |
| ²½Öč3£ŗČ”ŹŹĮæ²½Öč1ÖŠµÄ³ĮµķÓŚŹŌ¹ÜÖŠ£¬µĪ¼ÓĻ”ŃĪĖįĮ¬½Ó“ųČūµ¼Ęų¹Ü½«²śÉśµÄĘųĢåµ¼Čė³ĪĒåŹÆ»ŅĖ®ÖŠ£® | ³ĪĒåŹÆ»ŅĖ®±ä»ģ×Ē£®ĖµĆ÷øĆŹŌ¼ĮÖŠŗ¬ÓŠBaCO3 |
| ²½Öč4£ŗČ”²½Öč1ÖŠµÄĀĖŅŗÓŚÉÕ±ÖŠ£¬ÓĆpH¼Ę²āĘäpHÖµ | pHÖµĆ÷ĻŌ“óÓŚ9.6£¬ĖµĆ÷øĆŹŌ¼ĮÖŠŗ¬ÓŠBa£ØOH£©2£® |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | v£ØA£©=0.15mol/£ØL•min£© | B£® | v£ØB£©=0.04mol/£ØL•s£© | ||
| C£® | v£ØC£©=0.03mol/£ØL•s£© | D£® | v£ØD£©=0.4mol/£ØL•min£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
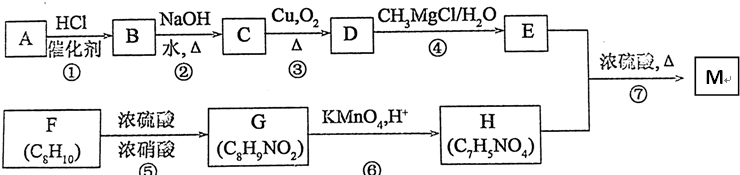
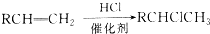
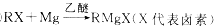
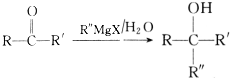
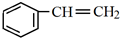 £¬CÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł£®
£¬CÖŠ¹ŁÄÜĶŵÄĆū³ĘĪŖōĒ»ł£®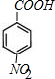 +
+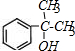 $?_{”÷}^{ÅØĮņĖį}$
$?_{”÷}^{ÅØĮņĖį}$ +H2O£®
+H2O£® ”¢
”¢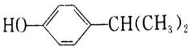 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | [ZnCl4]2-æռ乹ŠĶ³ŹĘ½ĆęĖıߊĪ | |
| B£® | [ZnCl4]2-æռ乹ŠĶ³ŹÕżĖÄĆęĢåŠĪ | |
| C£® | [ZnCl4]2-Ąė×ÓÖŠ“ęŌŚ2øö¦Ņ¼üŗĶ2øö¦Š¼ü | |
| D£® | [ZnCl3F]2-²»“ęŌŚ×ÅĶ¬·ÖŅģ¹¹Ģå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com