
(8分)下表是元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答下列问题。
族 周期 | ⅠA | 0 | |||||||
1 | H | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ⑤ | Ne | |||||||
3 | ① | ② | ③ | ④ | ⑥ |
(1)元素④的符号是 ;
(2)⑤和⑥两种元素原子半径的大小关系:⑤ ⑥(填“>”或“<”);
(3)①和②两种元素金属性强弱关系:① ②(填“>”或“<”);
(4)①的最高价氧化物的水化物与元素③的单质反应的化学方程式为: _ ________ _______。
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源:2014-2015学年上海市闵行区高三下学期质量调研考试(二模)化学试卷(解析版) 题型:推断题
(本题共14分)以下是由甲苯合成乙酰水杨酸和酚酞的合成路线。
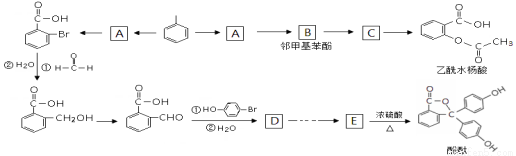
1.写出“甲苯→A”的化学方程式___________________________________________。
2.写出C的结构简式___________,E分子中的含氧官能团名称为__________________;
3.上述涉及反应中,“E→酚酞”发生的反应类型是______________。
4.写出符合下列条件的乙酰水杨酸的一种同分异构体的结构简式_________________。
(1)遇FeCl3溶液显紫色, (2)能与碳酸氢钠反应
(3)苯环上只有2个取代基的, (4)能使溴的CCl4溶液褪色。
5.写出乙酰水杨酸和NaOH溶液完全反应的化学方程式:
____________________________________________________________________。
6.由D合成E有多步,请设计出D→E的合成路线(有机物均用结构简式表示)。
(合成路线常用的表示方式为:D ……
…… E)
E)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省景德镇市高三下学期第三次质检考试理综化学试卷(解析版) 题型:推断题
【化学——选修5:有机化学基础】(15分)常用的油脂、蜡的漂白剂、化妆品助剂,橡胶硫化剂(C14H10O4,CAS号为94-36-0)已被禁用。下面是以物质A为原料合成C14H10O4,的流程:
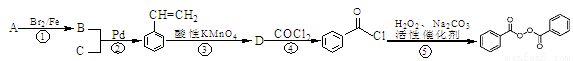
提示:①2010年赫克、根岸英一和铃木章因在“钯催化交叉偶联反应”研究领域作出了杰出贡献,而获得了诺贝尔化学奖,其反应机理可简单表示为: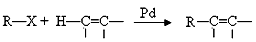
②苯乙烯和甲苯与酸性KMnO4溶液反应产物相同。
请回答下列问题:
(1)物质A的名称为 ,物质C中含有的官能团的名称为 ,D的结构简式为 ;
(2)反应①—④中属于取代反应的有 ;
(3)反应②的化学反应方程式 ;
(4)某物质E为漂白剂(C14H10O4)的同分异构体,同时符合下列条件的E的同分异构体有 种;
①含有联苯结构单元(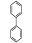 ),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH
),在一定条件下能发生银镜反应,且1molE最多可消耗4mol NaOH
②遇FeCl3溶液不显紫色,且苯环上核磁共振氢谱有六个吸收峰。
(5)请写出以苯乙烯和乙烯为原料,合成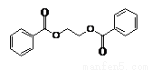 的流程,无机物任选,注明反应条件。示例如下:
的流程,无机物任选,注明反应条件。示例如下:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:填空题
(15分)蛇文石矿可以看作是由MgO、Fe2O3、Al2O3、SiO2组成。由蛇文石制取碱式碳酸镁的实验步骤如下:
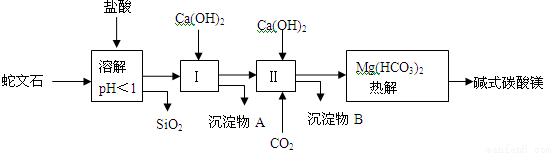
(1)蛇文石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是 。
(2)进行Ⅰ操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见下表)
氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
开始沉淀pH | 2.7 | 3.3 | 9.6 |
Ca(OH)2不能过量,若Ca(OH)2过量会导致 溶解、生成 沉淀。
(3)从沉淀混合物A中提取红色氧化物做颜料,先向沉淀物A中加入 (填物质的化学式),然后 (依次填写实验操作名称)。
(4)物质循环使用可节约能源。上述实验中,可以循环使用的物质是 (填写物质的名称)。
(5)设计一个实验,确定产品a MgCO3·b Mg(OH)2·cH2O中的a、b、c的值。将32.8g产品完全分解后,产生13.2g CO2和16.0g MgO。由此可知,产品的化学式中a∶b∶c= 。(填最简整数比)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省岳阳市高三质量检测(二)理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值。下列说法正确的是
A.一定条件下,1molN2和3molH2充分反应,生成物中的N-H键数目为6NA
B.完全燃烧1.5molCH3CH2OH和C2H4的混合物,转移电子数为18NA
C.100g 98%的浓硫酸中含氧原子个数为4NA
D.1L 0.1 mol/L的Na2S溶液中S2-和HS-的总数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三学业水平模拟考试化学试卷(解析版) 题型:选择题
下列物质,所含分子数最多的是(NA为阿伏加德罗常数)
A.10gH2 B.2molCl2 C.1.5NACO2 D.22.4LO2(标况下)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三普通高考测试(二)理综化学试卷(解析版) 题型:简答题
(16分)乙酰水杨酸是一种使用广泛的解热镇痛剂。合成原理是:
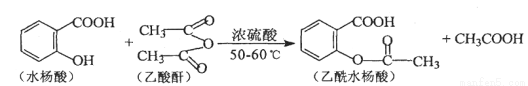
(1)乙酰水杨酸的分子式为 ,1mol乙酰水杨酸最多能与 mol H2 反应。
(2)上面反应的反应类型是 。
(3)有关水杨酸的说法,不正确的是 。
A.能与溴水发生取代反应和加成反应
B.可发生酯化反应和水解反应
C.1mol水杨酸最多能与2mol NaOH反应
D.遇 FeCl3溶液显紫色
(4)乙酰水杨酸与足量KOH溶液反应的化学方程式为 。
(5)乙酰氯(CH3COCl )也可以与水杨酸反应生成乙酰水杨酸,请写出化学反应方程式(不写条 件) 。
(6)写出一种符合下列条件的乙酰水杨酸的同分异构体的结构简式: 。
Ⅰ.能遇FeCl3溶液显色
Ⅱ.苯环上只有2种一溴取代物
Ⅲ.1mol该化合物能分别与含4mol Br2的溴水或4mol H2 反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省成都市高三4月模拟考理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,N表示粒子数。下列说法正确的是
A.0.1 mol苯乙烯中含有碳碳双键的数目为0.4NA
B.将1molCl2通入到水中,则N(HClO)+N(Cl-)+N(ClO-)=2[NA-N(Cl2)]
C.一定条件下,0.1 mol SO2与足量氧气反应生成SO3,转移电子数为0.2NA
D.电解精炼铜,当电路中通过的电子数目为0.2NA时,阳极质量减少6.4g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com