
【题目】甲醇﹣空气燃料电池(DMFC)是一种高效能、轻污染的车载电池,其工作原理如图.下列有关叙述正确的是( ) 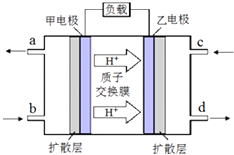
A.H+从正极区通过交换膜移向负极区
B.负极的电极反应式为:CH3OH(l)+H2O(l)﹣6e﹣=CO2(g)+6H+
C.d导出的是CO2
D.图中b、c分别是O2、甲醇
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】研究表明:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(As)元素,但它对人体是无毒的,砒霜的成分是As2O3,属剧毒物质,专家忠告:吃饭时不要同时大量食用海鲜和青菜,否则容易中毒,并给出了一个公式:大量海鲜+大量维生素C=砒霜.下面有关解释不正确的应该是
A.青菜中含有维生素C
B.维生素C具有还原性
C.致人中毒过程中砷发生还原反应
D.砒霜是氧化产物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】两种元素的核外电子层数之比与最外层电子数之比相等,则在核电荷数1~10的元素中,满足上述关系的元素共有( )
A.1对B.2对C.3对D.4对
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某物质中加入氢氧化钠溶液后加热产生能使湿润红色石蕊试纸变蓝的气体,若加入盐酸溶液,产生能使澄清石灰水变浑浊的气体,则该物质不可能是
A.NH4HCO3B.(NH4)2CO3C.(NH4)2SO4D.(NH4)2SO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】相同物质的量的Na、Fe、Al分别跟足量的稀硫酸反应,生成的气体在同温同压下体积比为
A.1:2:3B.46:56:27C.6:3:2D.1/23:1/28:1/9
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学药品与警示语对应正确的是( )
①酒精——剧毒品 ②浓硫酸——腐蚀品 ③汽油——易燃品 ④烧碱——剧毒品 ⑤氯酸钾——氧化剂 ⑥硝酸铵——爆炸品
A. ①②③⑥ B. ①②⑤ C. ①④⑤ D. ②③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】AlCl3是一种催化剂,某校学习小组用下面装置制备少量AlCl3。已知:AlCl3遇到空气中的水蒸气时能剧烈反应生成Al(OH)3和HCl;AlCl3在180℃时升华。根据要求完成下列问题:
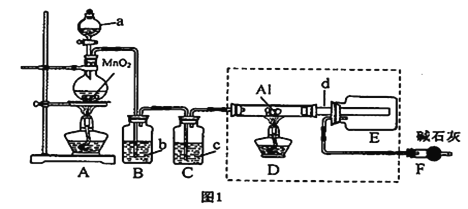
(1)A装置中反应的化学方程式为____________________________。
(2)试剂b为______________。
(3)所用d导管较粗的原因是______________;E装置的作用为______________。
(4)F装置的作用为______________。
(5)若图l中的D、E装置改为下面装置,D装置中的现象为_____________________;用离子方程式表示E中的现象变化____________________________。
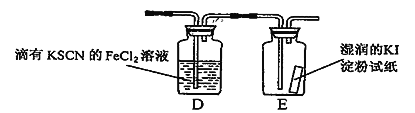
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组同学利用下图装置对电解氯化铜实验进行了研究。
装置 | 现象 |
| 电解一段时间时,阳极石墨表面产生气体,阴极石墨上附着红色物质,烧杯壁变热,溶液由蓝色变为绿色 |
(1)甲认为电解过程中阳极产生的是溶液变绿的原因,写出产生该物质的电极反应式:。
(2)乙查阅资料,CuCl2溶液中存在平衡:Cu2+ + 4Cl ![]() [CuCl4]2_(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因:。
[CuCl4]2_(黄色) ΔH>0。据此乙认为:电解过程中,[CuCl4]2_(黄色)浓度增大,与CuCl2蓝色溶液混合呈绿色。乙依据平衡移动原理推测在电解过程中[CuCl4]2_浓度增大的原因:。
(3)丙改用下图装置,在相同条件下电解CuCl2溶液,对溶液变色现象继续探究。
装置 | 现象 |
| 电解相同时间时,阳极石墨表面产生气泡,溶液仍为蓝色;阴极石墨上附着红色物质,溶液由蓝色变为绿色;U型管变热,冷却后阴极附近溶液仍为绿色 |
丙通过对现象分析证实了甲和乙的观点均不是溶液变绿的主要原因。丙否定甲的依据是 , 否定乙的依据是。
(4)丙继续查阅资料:
i. 电解CuCl2溶液时可能产生[CuCl2]_ , [CuCl2]_掺杂Cu2+后呈黄色
ii. 稀释含[CuCl2]_的溶液生成CuCl白色沉淀据此丙认为:电解过程中,产生[CuCl2]_掺杂Cu2+后呈黄色,与CuCl2蓝色溶液混合呈绿色。
丙进行如下实验:
a.取电解后绿色溶液2 mL,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
b. 另取少量氯化铜晶体和铜粉,向其中加2 mL浓盐酸,加热获得含[CuCl2]_的黄色溶液。
c. 冷却后向上述溶液……
d. 取c中2 mL溶液,加20 mL水稀释,静置5分钟后溶液中产生白色沉淀。
① a的目的是。
② 写出b中生成[CuCl2]_的离子方程式:。
③ 补充c中必要的操作及现象:。
丙据此得出结论:电解时阴极附近生成[CuCl2]_是导致溶液变绿的原因。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com