
【题目】火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水.当把 0.4mol 液态肼和 0.8mol H2O2 混合反应,生成氮气和水蒸气,放出 256.7kJ 的热量(相当于 25°C、101kPa下测得的热量)。(注:所有数值均保留小数点后一位)
(1)写出肼的结构式:_____________,过氧化氢电子式_____________。
(2)反应的热化学方程式为______________________________。
(3)已知 H2O(l)=H2O(g)ΔH=+44kJ/mol.则 16g 液态肼与液态双氧水反应生成液态水时放出的热量是_________ kJ。
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案科目:高中化学 来源: 题型:
【题目】已知:NH3·H2O(aq)与H2SO4(aq)反应生成1 mol正盐的ΔH=-24.2 kJ·mol-1;强酸、强碱稀溶液反应的中和热为ΔH=-57.3 kJ·mol-1。则NH3·H2O在水溶液中电离的ΔH等于
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1
C.+69.4 kJ·mol-1 D.+45.2 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下反应2AB(g)![]() A2(g)+B2(g)达到平衡状态的标志是
A2(g)+B2(g)达到平衡状态的标志是
A. 单位时间内生成nmolA2,同时消耗2n molAB
B. 容器内,3种气体AB、A2、B2共存
C. AB的消耗速率等于A2的消耗速率
D. 容器中各组分的体积分数不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下是部分共价键的键能数据:H—S 364 kJ·mol-1,S—S 266 kJ·mol-1,O===O 496 kJ·mol-1,H—O 463 kJ·mol-1。已知热化学方程式:
2H2S(g)+O2(g)===2S(g)+2H2O(g) ΔH1
2H2S(g)+3O2(g)===2SO2(g)+2H2O(g) ΔH2=-1 000 kJ·mol-1
反应产物中的S实为S8分子,是一个八元环状分子(如图所示)。
![]()
(1)试根据上述数据计算,ΔH1=________kJ·mol-1。
(2)将a mol H2S与b mol O2混合进行上述反应,当a>2b时,反应放热________kJ;将a mol H2S与b mol O2混合进行上述反应,当3a<2b时,反应放热________kJ。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质发生的变化,所克服的微粒间作用,属于同一类型的是
A.苯和己烷的挥发B.二氧化硅和生石灰的熔化
C.氯化钠和铁的熔化D.氯化钠和氯化氢的溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组气体通常情况下能稳定共存的是( )
A. NH3、O2、HCl B. N2、O2、HCl C. CO2、NO、O2 D. SO2、H2S、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的二元化合物,n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一元强酸,t通常是固态单质.上述物质的转化关系如图所示.下列说法正确的是( ) 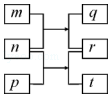
A.原子半径的大小W>X>Y
B.元素的非金属性Z>X>Y
C.X的氢化物常温常压下为液态
D.Y的最高价氧化物的水化物为弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组离子在水溶液中能够大量共存的是
A. OH -、 K+、NH4+ B. Ba2+、 SO42 -、H+
C. Ag+、 K+、Cl - D. Na+、 Cl -、 CO32 -
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】填空题
(1)I.比较原子半径的大小:OF;(填“>”或“<”,下同)
(2)比较酸性强弱:H3PO4H2SiO3
(3)稳定性:NH3PH3
(4)II.写出下列物质形成过程的电子式: HCl
(5)MgCl2 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com