
·ÖĪö ŹŌ¹ÜAµÄČÜŅŗÖŠµĪČė·ÓĢŖŹŌŅŗ³Ź·ŪŗģÉ«£¬ĖµĆ÷ČÜŅŗĻŌ¼īŠŌ£¬Ņ»¶Øŗ¬ÓŠOH-£¬øł¾ŻĄė×Ó¹²“ęŌĄķ£¬Ņ»¶ØƻӊAg+”¢Mg2+£¬Ņ»¶Øŗ¬ÓŠK+£®ŹŌ¹ÜBÖŠŅ»¶Øŗ¬ÓŠAg+”¢Mg2+£¬ŌņŅ»¶ØƻӊCl-£¬Ņ»¶Øŗ¬ÓŠNO3-£»
£Ø1£©øł¾ŻŅŌÉĻ·ÖĪöÅŠ¶ĻŹŌ¹ÜAµÄČÜŅŗÖŠ“ęŌŚµÄĄė×Ó£»ĀĮŗĶ¼īŅŗÉś³ÉĘ«ĀĮĖįŃĪŗĶĒāĘų£»
£Ø2£©øł¾ŻŹŌ¹ÜAŗĶBÖŠŗ¬ÓŠµÄĄė×Ó½ųŠŠ·ÖĪö£»
£Ø3£©øł¾Ż¹żĀĖŗóČÜŅŗÖŠ½öŗ¬ÓŠŅ»ÖÖČÜÖŹ£¬ĒŅµĆµ½ĻąÓ¦µÄ½šŹō½ųŠŠ·ÖĪö£»
£Ø4£©øł¾ŻA”¢BČÜŅŗÖŠ“ęŌŚµÄĄė×ÓŠĪ³É·“Ó¦µÄĄė×Ó·½³ĢŹ½£»
£Ø5£©·Ö±šµĪ¼ÓŃĪĖįŗĶÉŁĮæBa£ØOH£©2£¬ĒāĄė×ÓŗĶĢ¼ĖįĒāøłĄė×ÓÉś³ÉĖ®ŗĶ¶žŃõ»ÆĢ¼£¬Ģ¼ĖįĒāøłĄė×ÓÓėĒāŃõ»Æ±µČÜŅŗ·“Ӧɜ³ÉĢ¼Ėį±µ³ĮµķŗĶĢ¼ĖįøłĄė×Ó£¬¾Ż“ĖŹéŠ“Ąė×Ó·½³ĢŹ½£®
½ā“š ½ā£ŗĻņŹŌ¹ÜAµÄČÜŅŗÖŠµĪČė·ÓĢŖŹŌŅŗ³Ź·ŪŗģÉ«£¬ĖµĆ÷ČÜŅŗĻŌ¼īŠŌ£¬Ņ»¶Øŗ¬ÓŠOH-£¬øł¾ŻĄė×Ó¹²“ęŌĄķ£¬Ņ»¶ØƻӊAg+”¢Mg2+£¬Ņ»¶Øŗ¬ÓŠK+£®ŹŌ¹ÜBÖŠŅ»¶Øŗ¬ÓŠAg+”¢Mg2+£¬ŌņŅ»¶ØƻӊCl-£¬Ņ»¶Øŗ¬ÓŠNO3-£»
£Ø1£©ŹŌ¹ÜAÖŠŗ¬ÓŠK+”¢OH-”¢Cl-£¬ŹŌ¹ÜBÖŠŗ¬ÓŠAg+”¢Mg2+”¢NO3-£¬ČōĻņAČÜŅŗÖŠ¼ÓČėĀĮʬ£¬ĀĮŗĶ¼īŅŗÉś³ÉĘ«ĀĮĖįŃĪŗĶĒāĘų£¬·“Ó¦ĪŖ£ŗ2Al+2OH-+2H2O=2AlO2-+3H2”ü£¬
¹Ź“š°øĪŖ£ŗK+”¢OH-”¢Cl-£»2Al+2OH-+2H2O=2AlO2-+3H2”ü£»
£Ø2£©ČōĻņijŹŌ¹ÜÖŠµĪČėĻ”ŃĪĖį²śÉś³Įµķ£¬ŌņøĆŹŌ¹ÜÖŠŗ¬ÓŠAg+£¬ĪŖŹŌ¹ÜB£¬¹Ź“š°øĪŖ£ŗB£»
£Ø3£©ČōĻņŹŌ¹ÜBµÄČÜŅŗÖŠ¼ÓČėŗĻŹŹµÄŅ©Ę·ŗ󣬹żĀĖŗóČÜŅŗÖŠ½öŗ¬ÓŠŅ»ÖÖČÜÖŹ£¬ĒŅµĆµ½ĻąÓ¦µÄ½šŹō£¬Ó¦øĆ·¢ÉśÖĆ»»·“Ó¦£¬ĒŅ²»ŅżČėĘäĖūĄė×Ó£¬Ōņ¼ÓČėŅ©Ę·ŹĒMg£¬·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗMg+2Ag+=2Ag+Mg2+£»
¹Ź“š°øĪŖ£ŗMg Mg+2Ag+=2Ag+Mg2+£»
£Ø4£©Čō½«ŹŌ¹ÜAŗĶŹŌ¹ÜBÖŠµÄČÜŅŗ°“Ņ»¶ØĢå»ż±Č»ģŗĻ¹żĀĖŗó£¬ÕōøÉĀĖŅŗæɵƵ½Ņ»ÖÖ“æ¾»Īļ£¬ŌņAg+ÓėCl-Ē”ŗĆĶźČ«·“Ó¦£¬Mg2+ŗĶOH-Ē”ŗĆĶźČ«·“Ó¦£¬Ź£Óą¼ŲĄė×ÓŗĶĻõĖįøłĄė×Ó£¬»ģŗĻ¹ż³ĢÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗAg++Cl-=AgCl”ż”¢Mg2++2OH-=Mg£ØOH£©2”ż£¬¹Ź“š°øĪŖ£ŗAg++Cl-=AgCl”ż£»Mg2++2OH-=Mg£ØOH£©2”ż£»
£Ø5£©ČōĻņŹŌ¹ÜAµÄČÜŅŗÖŠµÄŃōĄė×Ó×é³ÉµÄĢ¼ĖįĒāŃĪČÜŅŗÖŠ£¬·Ö±šµĪ¼ÓŃĪĖįŗĶÉŁĮæBa£ØOH£©2£¬Ōņ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ£ŗHCO3-+H+=H2O+CO2”ü£¬Ba2++2OH-+2HCO3-=BaCO3”ż+CO32-+2H2O£¬¹Ź“š°øĪŖ£ŗHCO3-+H+=H2O+CO2”ü£»Ba2++2HCO3-+2OH-=BaCO3”ż+CO32-+2H2O£®
µćĘĄ ±¾Ģāæ¼²éĮĖĄė×Ó¹²“ę¼°Ąė×Ó·½³ĢŹ½µÄŹéŠ“£¬ĢāÄæÄѶČÖŠµČ£¬ŹŌĢāÉę¼°µÄÄŚČŻ½Ļ¶ą£¬³ä·Öæ¼²éĮĖѧɜ¶ŌĖłŃ§ÖŖŹ¶µÄÕĘĪÕĒéæö£»×¢ŅāÕĘĪÕĄė×Ó·“Ó¦·¢ÉśµÄĢõ¼ž¼°Ąė×Ó·½³ĢŹ½µÄŹéŠ“·½·Ø£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā

| A£® | ¢ŁÖŠÉś³É7molH2O | B£® | ¢ŚÖŠÉś³É2molCO2 | ||
| C£® | ¢ŪÖŠ×ī¶ąĻūŗÄ3molBr2 | D£® | ¢ÜÖŠ×ī¶ąĻūŗÄ7molH2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
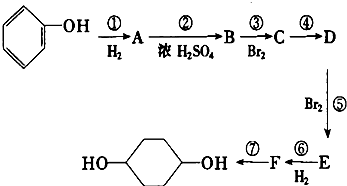
 ӢD
”¢D £®
£®
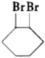 +2NaOH$”ś_{”÷}^{ŅŅ“¼}$
+2NaOH$”ś_{”÷}^{ŅŅ“¼}$ +2NaBr+2H2O
+2NaBr+2H2O £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øĆŌŖĖŲæÉÄÜÓŠ·ÅÉäŠŌ | |
| B£® | øĆŌŖĖŲĪ»ÓŚŌŖĖŲÖÜĘŚ±ķÖŠµÄµŚIIA×å | |
| C£® | ĘäÖŠ×ÓŹżÓėÖŹ×ÓŹżÖ®²īĪŖ165 | |
| D£® | ĘäŌ×ÓÖŹĮæŹĒ12CŌ×ÓÖŹĮæµÄ277±¶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | n+1 | B£® | n+2 | C£® | n+3 | D£® | n+5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| ·ÖĄą±ź×¼ | Äܵ¼µē | ·Ēµē½āÖŹ | µē½āÖŹ |
| ŹōÓŚøĆĄąµÄĪļÖŹ | ¢Ś¢ß¢ą¢į | ¢Ü | ¢Ū¢Ż¢Ž¢į |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
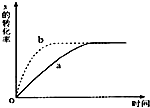 ČēĶ¼ĒśĻßa±ķŹ¾·ÅČČ·“Ó¦ X£Øg£©+Y£Øg£©?Z£Øg£©+M£Øg£©+N£Øs£©½ųŠŠ¹ż³ĢÖŠXµÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄ¹ŲĻµ£®ČōŅŖøıäĘšŹ¼Ģõ¼ž£¬Ź¹·“Ó¦¹ż³Ģ°“bĒśĻß½ųŠŠ£¬æɲÉČ”µÄ“ėŹ©ŹĒ£Ø””””£©
ČēĶ¼ĒśĻßa±ķŹ¾·ÅČČ·“Ó¦ X£Øg£©+Y£Øg£©?Z£Øg£©+M£Øg£©+N£Øs£©½ųŠŠ¹ż³ĢÖŠXµÄ×Ŗ»ÆĀŹĖꏱ¼ä±ä»ÆµÄ¹ŲĻµ£®ČōŅŖøıäĘšŹ¼Ģõ¼ž£¬Ź¹·“Ó¦¹ż³Ģ°“bĒśĻß½ųŠŠ£¬æɲÉČ”µÄ“ėŹ©ŹĒ£Ø””””£©| A£® | ÉżøßĪĀ¶Č | B£® | ¼Ó“óXµÄĶ¶ČėĮæ | C£® | ĖõŠ”Ģå»ż | D£® | ¼õŠ”NµÄĶ¶ČėĮæ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com