
苯甲酸广泛应用于制药和化工行业,某兴趣小组同学利用高锰酸钾氧化甲苯制备苯甲酸(KMnO4中性条件下还原产物为MnO2,酸性条件下为Mn2+)

已知:苯甲酸相对分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 go。

实验流程:
①往装置A中加入2.7mL (2.3 g)甲苯和125 mL水,然后分批次加入8.5 g稍过量的KMnO4固体,控制反应温度约在100℃,当甲苯层近乎消失,回流不再出现油珠时,停止加热。
②将反应混合物趁热过滤,用少量热水洗涤滤渣,合并滤液与洗涤液,冷却后加入浓盐酸,经操作I得白色较干燥粗产品。
③纯度测定:称取1.220g白色样品,配成100mL、甲醇溶液,取25.00mL溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示列举

请回答:
(1)装置A的名称????????? 。若不用温度计,本实验控制反应温度的措施为?????????? 。
(2)白色粗产品中除了KCl外,其他可能的无机杂质为____???????????? 。
(3)操作I的名称?????????????????????????????????? 。
(4)步骤③中用到的定量仪器有?????????????? ,100mL容量瓶,50mL酸式、碱式滴定管。
(5)样品中苯甲酸纯度为??????????????????????????? 。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果??? (填“偏大”、“偏小”或“不变”)。
(1)三颈烧瓶(1分),沸水浴加热或者加热保持反应液处于沸腾(2分,仅答水浴加热得1分)
(2)MnCl2(2分)
(3) 过滤、干燥或抽滤(2分)
(4) 分析天平(2分)
(5) 0.9600或96.00%(2分)?? (6)偏小(2分)
【解析】
试题分析:(1)本实验控制反应温度约在100℃,可以采用水浴加热。(2)实验使用了KMnO4做氧化剂,白色粗产品中除了KCl外,还有MnCl2。(3)从混合液中得到沉淀一般采用过滤、干燥,也可以采用抽滤的方法。(4)步骤③的称量需要精确度高的分析天平才能保证精确度。
(5)舍弃第三次数据,平均消耗体积为24.00mL,又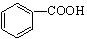 ~NaOH,滴定的n(
~NaOH,滴定的n( )= 0.1000mol/L×24.00×10-3L=2.400×10-3 mol;而配制溶液用的是测定的4倍,即测定含样品0.3050g,所以,样品中苯甲酸纯度为
)= 0.1000mol/L×24.00×10-3L=2.400×10-3 mol;而配制溶液用的是测定的4倍,即测定含样品0.3050g,所以,样品中苯甲酸纯度为 =0.9600。
=0.9600。
(6)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视,两次度数距离偏小,测定结果也偏小。
考点:化学实验设计与定量测定。


科目:高中化学 来源: 题型:
| △ |

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解, 冷却 冷却 过滤 过滤 |
得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中, 滴入适量的硝酸酸化的AgNO3溶液 滴入适量的硝酸酸化的AgNO3溶液 |
生成白色沉淀 | 滤液含Cl- |
| ③ | 干燥白色晶体, 加热使其融化,测其熔点 加热使其融化,测其熔点 |
熔点为122.4℃ 熔点为122.4℃ |
白色晶体是苯甲酸 |
| 2.4×10-3mol×4×122g/mol |
| 1.22g |
| 2.4×10-3mol×4×122g/mol |
| 1.22g |
查看答案和解析>>
科目:高中化学 来源:2013-2014学年江苏省苏北四市高三上期末统考化学试卷(解析版) 题型:填空题
苯甲酸广泛应用于制药和化工行业。某化学小组用甲苯作主要原料制备苯甲酸,反应过程如下:
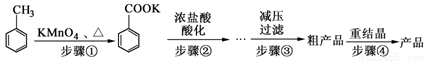
甲苯、苯甲酸钾、苯甲酸的部分物理性质见下表:
|
物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
在水中溶解性 |
|
甲苯 |
-95 |
110.6 |
0.8669 |
难溶 |
|
苯甲酸钾 |
121.5~123.5 |
|
|
易溶 |
|
苯甲酸 |
122.4 |
248 |
1.2659 |
微溶 |
(1)将步骤①得到混合物加少量水,分离有机相和水相。有机相在 (填“上”或“下”)层;实验操作的名称是 。
(2)步骤②用浓盐酸酸化的目的是 。
(3)减压过滤装置所包含的仪器除减压系统外,还有 、 (填仪器名称)。
(4)已知温度越低苯甲酸的溶解度越小,但为了得到更多的苯甲酸晶体,重结晶时并非温度越低越好,理由是 。
(5)重结晶时需要趁热过滤,目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
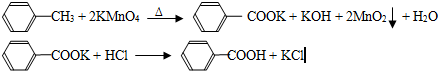
苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸,反应原理:
![]()
![]()
![]() CH3 + 2KMnO4 Δ COOK + KOH + 2MnO2 + H2O
CH3 + 2KMnO4 Δ COOK + KOH + 2MnO2 + H2O
![]()
![]()
![]() COOK + HCl COOH + KCl
COOK + HCl COOH + KCl
|
|
|
|
|
|
|
|
| |||||
|
|
已知:苯甲酸分子量122,熔点122.4℃,在25℃和95℃时溶解度分别为0.3 g和6.9 g;纯净固体有机物都有固定熔点。
(1)操作Ⅰ为 ,操作Ⅱ为 。
(2)无色液体A是 ,定性检验A的试剂是 ,现象是
。
(3)测定白色固体B的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体B是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请在答题卡上完成表中内容。
| 序号 | 实验方案 | 实验现象 | 结论 |
| ① | 将白色固体B加入水中,加热溶解,
| 得到白色晶体和无色溶液 | |
| ② | 取少量滤液于试管中, | 生成白色沉淀 | 滤液含Cl— |
| ③ | 干燥白色晶体, |
| 白色晶体是苯甲酸 |
(4)纯度测定:称取1.220g产品,配成100ml甲醇溶液,移取25.00ml溶液,滴定,消耗KOH的物质的量为2.40×10—3mol,产品中苯甲酸质量分数的计算表达式为 ,计算结果为 (保留二位有效数字)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com