
【题目】已知X、Y、Z、W为短周期元素,X的一种核素的质子数为8;Y和Ne原子的核外电子数相差1;Z的单质是一种常见的半导体材料;W的非金属性在同周期元素中最强。其原子半径随原子序数变化如图所示。
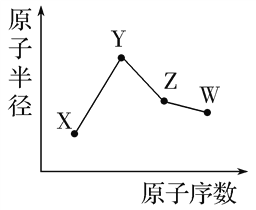
下列说法正确的是
A.对应简单离子半径:W>Y>X
B.对应气态氢化物的稳定性:Z>W
C.化合物YWX中既含离子键,又含共价键
D.Z的氧化物能与W的气态氢化物、Y的最高价氧化物对应水化物的溶液反应
 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:
【题目】下列实验装置能达到实验目的是(夹持仪器未画出)
A.  用于检验溴乙烷消去生成的乙烯
用于检验溴乙烷消去生成的乙烯
B.  用于石油的分馏
用于石油的分馏
C.  用于实验室制硝基苯
用于实验室制硝基苯
D. 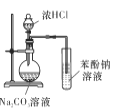 可证明酸性:盐酸>碳酸>苯酚
可证明酸性:盐酸>碳酸>苯酚
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有①氨水 ②NH4Cl溶液 ③Na2CO3溶液 ④NaHCO3溶液各25 mL,物质的量浓度均为0.1 mol/L,下列说法正确的是
A. 4种溶液pH的大小顺序:①>④>③>②
B. 溶液①、②等体积混合后pH > 7,则c(NH4+) < c(NH3·H2O)
C. 向溶液①、②中分别加入25 mL 0.1mol/L盐酸后,溶液中c(NH4+):①>②
D. 向溶液③、④中分别加入12.5 mL 0.1mol/L NaOH溶液后,两溶液中的离子种类相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氧化氯(ClO2)是一种高效消毒剂,易溶于水,沸点为11.0℃,极易爆炸分解,若用空气、二氧化碳、氮气等惰性气体稀释时,爆炸性则降低。用干燥的氯气与固体亚氯酸钠制备二氧化氯,装置如图:
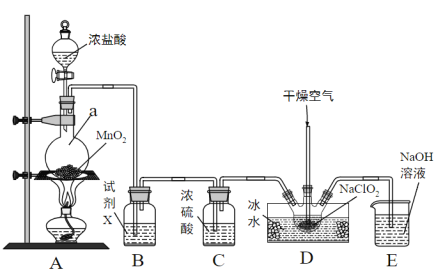
(1)仪器a的名称为___________,装置A中反应的离子方程式为____________________。
(2)试剂X的作用是_____________________________。
(3)装置D中通入干燥空气的作用是______________________________。
(4)该实验装置的缺陷是_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方案中,能达到相应实验目的的是
实验方案 |
|
|
|
|
目的 | A.比较乙醇分子中羟基氢原子和水分子中氢原子的活泼性 | B.除去乙烯中的二氧化硫 | C.制银氨溶液 | D.证明碳酸酸性强于苯酚 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是
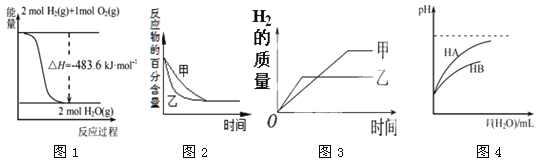
A.图1表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为241.8 kJ·mol-1
B.图2表示压强对可逆反应2A(g)+2 B(g)![]() 3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
C.图3表示等质量的钾、钠分别与足量水反应,则甲为钠
D.图4表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则相同条件下NaA溶液的pH大于同浓度的NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,在20mL0.1mol/L HR 溶液中滴加0.1000mol/LNaOH溶液,混合溶液的PH与所加NaOH溶液体积的关系如图所示。下列推断正确的是
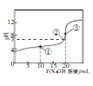
A. ①、②、③三点中,③对应的溶液中c水(H+)·c水(OH-)最大
B. HR溶液中只存在H+、R-、OH-、H2O四种微粒
C. ②点溶液中一定存在c(Na+)>c(R-)>c(H+)=c(OH-)
D. NaR的水解常数Ka和水解程度:③>②>①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。下列说法正确的是
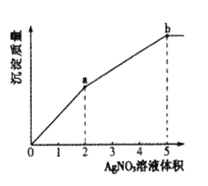
A.KSP (AgCl) < KSP (AgI)
B.c( Cl- ) :c( I-) =3:2
C.m( AgCl ) :m( AgI ) =" 2" :3
D.a~b段产生黄色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】合成氨工业在工农业生产、生活中有着重要作用。反应原理为:3H2(g)+N2(g)![]() 2NH3(g) △H < 0。
2NH3(g) △H < 0。
(1)在T ℃时,将一定物质的量的H2和N2置于一容积不变的密闭容器中。
①下列各项能说明该反应已达到平衡状态的是__________(填序号)。
a.容器内的压强不再随时间变化
b.3υ(N2)=υ(H2)
c.3υ正(H2)=2υ逆(NH3)
d.混合气体的密度保持不变
②达上述平衡后,其他条件不变,升高温度,υ逆___________________(填“增大”、“不变”、“减小”),υ正和υ逆的关系为υ正___________υ逆(填:“>”、“=”、“<”),最后二者相等。
③该条件下达到平衡时,向容器内充入惰性气体,增大容器内的压强,NH3的体积分数将(填:“变大”、“不变”或“变小”)。________
(2)在T ℃时,将一定物质的量的H2和N2置于一容积可变的密闭容器中。达到平衡后,改变某一条件使反应速率发生了如图所示的变化,改变的条件可能是______。
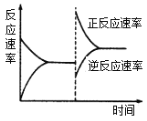
a.升高温度,同时加压b.降低温度,同时减压
c.保持温度、压强不变,增大反应物浓度
d.保持温度、压强不变,减小生成物浓度
(3)在T ℃时,将0.6 mol H2和0.4 mol N2置于容积为2 L的密闭容器中发生反应:3H2(g)+N2(g)![]() 2NH3 (g) △H <0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强(MPa)随时间变化如图所示:8 min内NH3的平均生成速率为_______。
2NH3 (g) △H <0。若保持温度不变,某兴趣小组同学测得反应过程中容器内压强(MPa)随时间变化如图所示:8 min内NH3的平均生成速率为_______。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com