
 B是化学实验室中最常见的有机物,其产量可以用来衡量一个国家的石油化工发展水平,还是一种植物生长调节剂.并能进行如图所示的反应.且D能发生加聚反应.
B是化学实验室中最常见的有机物,其产量可以用来衡量一个国家的石油化工发展水平,还是一种植物生长调节剂.并能进行如图所示的反应.且D能发生加聚反应. .
. 分析 B的产量通常用来衡量一个国家石油化工水平,还是一种植物生长调节剂,则B是乙烯,乙烯与氢气发生加成反应生成C为乙烷,A与氢气发生加成反应生成乙烯,故A为乙炔,乙炔与HCl发生加成反应生成D,D可以发生加聚反应,故D为CH2=CHCl,乙炔与溴发生加成反应生成1,1,2,2-四溴乙烷,以此来解答.
解答 解:B的产量通常用来衡量一个国家石油化工水平,还是一种植物生长调节剂,则B是乙烯,乙烯与氢气发生加成反应生成C为乙烷,A与氢气发生加成反应生成乙烯,故A为乙炔,乙炔与HCl发生加成反应生成D,D可以发生加聚反应,故D为CH2=CHCl,乙炔与溴发生加成反应生成1,1,2,2-四溴乙烷,
(1)A为乙炔,含有碳碳三键,其结构简式为HC≡CH,故答案为:HC≡CH,故答案为:HC≡CH;
(2)乙炔与氢气发生加成反应生成乙烯,反应方程式为HC≡CH+H2→CH2=CH2,故答案为:HC≡CH+H2→CH2=CH2;
(3)乙炔与足量的溴水反应的方程式为:HC≡CH+2Br2→Br2CHCHBr2,产物名称为:1,1,2,2-四溴乙烷,
故答案为:HC≡CH+2Br2→Br2CHCHBr2;1,1,2,2-四溴乙烷;
(4)D为氯乙烯,含有碳碳双键,在一定条件下发生加聚反应生成聚氯乙烯,反应化学反应方程式为:n CH2=CHCl$\stackrel{催化剂}{→}$ ,
,
故答案为:n CH2=CHCl$\stackrel{催化剂}{→}$ .
.
点评 本题考查有机物推断、有机反应类型、有机物命名、有机方程式书写等,难度不大,涉及炔、烯烃的性质与转化,注意对基础知识的理解掌握.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 在稀硫酸中加入铜粉,铜粉不溶解,再加入Cu(NO3)2固体,铜粉仍不溶解 | |
| B. | 某气体能使湿润的红色石蕊试纸变蓝,该气体的水溶液一定显碱性 | |
| C. | 铜与稀硝酸反应的离子方程式为3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O | |
| D. | HNO3→NO→NO2,以上各步变化均能通过一步实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 稀硝酸、稀硫酸均能将木炭氧化成二氧化碳 | |
| B. | Na2O2与水反应,红热的Fe与水蒸气反应均能生成气体 | |
| C. | Li、C、P分别在足量氧气中燃烧均生成一种相应氧化物 | |
| D. | NaHCO3、Na2CO3、(NH4)2CO3三种固体受热后均能生成气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
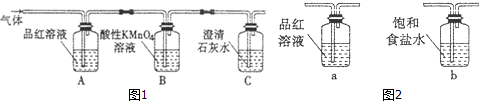
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
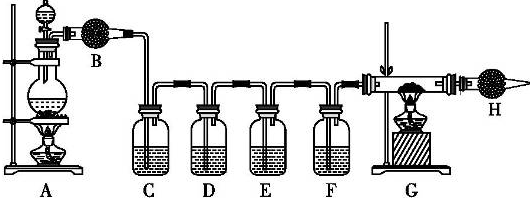
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PE和PVC制成的保鲜膜均有毒,不能用于保鲜食品 | |
| B. | 乙烯、聚乙烯和聚氯乙烯均能与溴水发生加成反应,使之褪色 | |
| C. | 上述流程中A是ClCH2CH2Cl,B是CH2═CHCl | |
| D. | ①②③④四步反应中,无消去反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.01% | B. | 0.1% | C. | 0.2% | D. | 1% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com