
| t�� | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |

| ��ѧʽ | ����ƽ�ⳣ�� |
| HCN | K=4.9��10-10 |
| H2CO3 | K1=4.3��10-7��K2=5.6��10-11 |
���� ��1����a����ѧƽ�ⳣ������ָ��һ���¶��£����淴Ӧ�ﵽƽ��ʱ��������Ũ�ȵĻ�ѧ���������ݵij˻����Ը���Ӧ��Ũ�ȵĻ�ѧ���������ݵij˻����õı�ֵ��
��b����μӷ�Ӧ�Ķ�����̼Ϊxmol����������ʽ��ʾ��ƽ��ʱ����ֵ����ʵ��������ڷ�Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ��������ƽ�ⳣ���з��̼�����
��2����a����ͼ��֪����Ӧ����������������������Ϊ���ȷ�Ӧ��
��b�����ݸ�˹���ɣ����ͼ��֪1molNH4+��aq��ȫ��������NO3-��aq���ų�������Ϊ273kJ+73kJ=346kJ��ע���ۼ�״̬����Ӧ�ȣ���д�Ȼ�ѧ����ʽ��
��3������HCN�ĵ���ƽ�ⳣ��Ka=$\frac{c��{H}^{+}��•c��C{N}^{-}��}{c��HCN��}$����֪$\frac{c��HCN��}{c��C{N}^{-}��}$=$\frac{c��{H}^{+}��}{{K}_{a}}$���ݴ˼��㣻
��̼���һ�����볣������HCN�ģ��������볣��С��HCN�ģ���̼�������ǿ��HCN��Ϊ̼���������������HCN������NaCN��Һ��ͨ������CO2����Ӧ����HCN��NaHCO3��
��4��̼���ƺ��Ȼ��Ʒ�Ӧ������̼��Ƴ�������Һ��̼���ʣ�࣬��������Һ��ʣ��̼�������Ũ�ȣ�����Ksp=c��CO32-��•c��Ca2+����������Һ��c��Ca2+����
��� ��1����a�����淴Ӧ��CO2��g��+H2��g��?CO��g��+H2O��g������ƽ�ⳣ������ʽK=$\frac{c��CO��•c��{H}_{2}O��}{c��C{O}_{2}��•c��{H}_{2}��}$��
�ʴ�Ϊ��$\frac{c��CO��•c��{H}_{2}O��}{c��C{O}_{2}��•c��{H}_{2}��}$��
��b����μӷ�Ӧ�Ķ�����̼Ϊxmol����
CO2��g��+H2��g��?CO��g��+H2O��g��
��ʼ��mol����1 1 0 0
ת����mol����x x x x
ƽ�⣨mol����1-x 1-x x x
���ڷ�Ӧǰ������������䣬���������ʵ�������Ũ�ȼ���ƽ�ⳣ������$\frac{x��x}{��1-x������1-x��}$=1�����x=0.5��
�ʶ�����̼��ת����Ϊ$\frac{0.5mol}{1mol}$��100%=50%��
�ʴ�Ϊ��50%��
��2����a����ͼ��֪����Ӧ����������������������Ϊ���ȷ�Ӧ��
�ʴ�Ϊ�����ȣ�
��b�����ݸ�˹���ɣ����ͼ��֪1molNH4+��aq��ȫ��������NO3-��aq���ų�������Ϊ273kJ+73kJ=346kJ����Ӧ�Ȼ�ѧ����ʽΪ��NH4+ ��aq��+2O2��g���TNO3- ��aq��+2H+��aq��+H2O��l����H=-346 kJ/mol��
�ʴ�Ϊ��NH4+ ��aq��+2O2��g���TNO3- ��aq��+2H+��aq��+H2O��l����H=-346 kJ/mol��
��3������HCN�ĵ���ƽ�ⳣ��Ka=$\frac{c��{H}^{+}��•c��C{N}^{-}��}{c��HCN��}$����֪$\frac{c��HCN��}{c��C{N}^{-}��}$=$\frac{c��{H}^{+}��}{{K}_{a}}$=$\frac{1{0}^{-11}}{4.9��1{0}^{-10}}$mol/L��2.0��10-2
mol/L��
�ʴ�Ϊ��2.0��10-2��
��̼���һ�����볣������HCN�ģ��������볣��С��HCN�ģ���̼�������ǿ��HCN��Ϊ̼���������������HCN������NaCN��Һ��ͨ������CO2����Ӧ����HCN��NaHCO3���÷�Ӧ���ӷ���ʽΪ��CN-+CO2+H2O=HCN+HCO3-��
�ʴ�Ϊ��CN-+CO2+H2O=HCN+HCO3-��
��4��̼���ƺ��Ȼ��Ʒ�Ӧ������̼��Ƴ�������Һ��̼���ʣ�࣬ʣ��̼������ӵ����ʵ���Ũ��Լ�ǣ�$\frac{0.4V-0.2V}{2V}$=0.1mol/L������Ksp=c��Ca2+��•c��CO32-������֪c��Ca2+��=$\frac{Ksp}{c��C{{O}_{3}}^{2-}��}$=4.96��10-8 ��mol/L����
�ʴ�Ϊ��4.96��10-8��
���� ��������ƴ������Ŀ���漰��ѧƽ�ⳣ�����йؼ��㡢�Ȼ�ѧ����ʽ��д������ƽ�ⳣ��Ӧ�ü��йؼ��㡢�ܶȻ��йؼ��㣬��4����ע�����̼�������Ũ�ȣ��Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
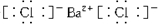 ���۵ĵ���ʽ��
���۵ĵ���ʽ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 40 | B�� | 41 | C�� | 42 | D�� | 48 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҷ�����ˮ��Һ���̵�ܵͣ����������������Ŀ����� | |
| B�� | �������ķе���Ҷ����ķе�ߣ����������ƻ�ױƷ | |
| C�� | �����ֶ�Ԫ����������ˮ�����������л��ܼ� | |
| D�� | ��������������ըҩ���Ҷ������Ƶ��ڵ���Ҫԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��BA2�Ľṹʽ�ǣ�S=C=S��
��BA2�Ľṹʽ�ǣ�S=C=S���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
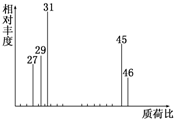 Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺
Ϊ�˲ⶨij�л���A�Ľṹ��������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��FeI2����Һ�У�ͨ������Cl2��2Fe2++2I-+2Cl2�TI2+2Fe3++4Cl- | |
| B�� | Fe��OH��3��������Fe��OH��3+3H+�TFe3++3H2O | |
| C�� | ��ˮ������ͨ�������CO2��SiO32-+2CO2+2H2O�TH2SiO3��+2HCO3- | |
| D�� | ����������KIO3��Һ��KI��Һ������Ӧ����I2��IO3-+5I-+3H2O�T3I2+6OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
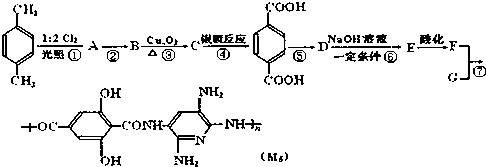
 ��
�� ��F�ĺ��������ŵ��������Ȼ������ӣ��ǻ���
��F�ĺ��������ŵ��������Ȼ������ӣ��ǻ��� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com