
用已知浓度的NaOH标准液滴定未知浓度的醋酸溶液,下列操作会导致测定结果偏高的是
A.以甲基橙为指示剂滴至溶液由红色变橙色
B.滴定前碱式滴定管尖嘴处有气泡,滴定后气泡消失
C.读滴定管读数时,滴定前仰视,终点时俯视
D.振荡时锥形瓶中的液滴溅出来
科目:高中化学 来源:2016-2017学年山东省菏泽市高二上学期期中化学试卷(解析版) 题型:选择题
在四个不同的容器中进行化学反应4A(g)+5B(g) 4C(g)+6D(g),以下是在不同容器中分别用不同物质表示的化学反应速率,所表示反应速率最快的
4C(g)+6D(g),以下是在不同容器中分别用不同物质表示的化学反应速率,所表示反应速率最快的
A.v(A)=0.36mol•L-1•s-1 B.v(B)=0.55mol•L-1•s-1
C.v(C)=0.40mol•L-1•s-1 D.v(D)=0.48mol•L-1•s-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上学期期中化学试卷(解析版) 题型:填空题
根据下列化合物:①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O。回答下列问题。
(1)NH4Cl溶液显__________性,用离子方程式表示原因 , 其溶液中离子浓度大小顺序为_________
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=__________mol/L在pH=3的CH3COOH溶液中,水电离出来的c(H+)=__________mol/L。
(3)已知纯水中存在如下平衡:H2O H++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是_____________(填字母序号)。
H++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是_____________(填字母序号)。
A.向水中加入NaHSO4固体 B.向水中加Na2CO3固体
C.加热至100℃ D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH和⑦NH3·H2O分别加水稀释m倍、n倍,稀 释后两种溶液的pH仍相等,则m__________n(填“<”、“>”或“=”)。
(5)①NaCl、②NaOH、③HCl、⑤CH3COONa、⑥CH3COOH,这5种溶液的物质的量浓度相同,则这5种溶液按 pH由大到小的顺序为:______________(填序号)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年内蒙古高二上学期期中化学试卷(解析版) 题型:选择题
在0.1 mol/L CH3COOH溶液中存在如下电离平衡:CH3COOH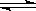 CH3COO-+H+,对于该平衡,下列叙述正确的是( )
CH3COO-+H+,对于该平衡,下列叙述正确的是( )
A.加入水时,平衡向逆反应方向移动
B.加入少量NaOH固体,平衡向正反应方向移动
C.加入少量0.1 mol/L HCl溶液,溶液中c(H+)不变
D.加入少量CH3COONa固体,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃
B.分子组成符合CnH2n+2的烃一定是烷烃
C.正戊烷分子中 所有原子均在一条直线上
所有原子均在一条直线上
D.CH3CH(CH3)2在光照下与氯气反应,可以生成四种一氯代烃
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
Cu(OH)2在水中存在着如下沉淀溶解平衡:Cu(OH)2(s) 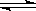 Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
Cu2+(aq)+2OH-(aq),在常温下,Ksp=2×10-20。某CuSO4溶液中,c(Cu2+)=0.02 mol·L-1,在常温下如果要生成Cu(OH)2沉淀,需要向CuSO4溶液加入碱溶液来调整pH,使溶液的pH大于( )
A.2  B.3 C.4 D.5
B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源:2016-2017学年辽宁省高二上期中化学试卷(解析版) 题型:选择题
下列有关电解质溶液的说法正确的是
 A.分别测等浓度的醋酸和氨水pH ,发现二者的pH 之和为14,说明常温下醋酸和氨水的电离平衡常数相等
A.分别测等浓度的醋酸和氨水pH ,发现二者的pH 之和为14,说明常温下醋酸和氨水的电离平衡常数相等
B.将CH3COONa溶液从25℃ 升温至 40℃ ,溶液中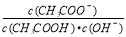 增大
增大
C.向硝酸中加入氨水至中性,溶液中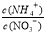 <1
<1
D.向AgCl、AgBr 的饱和溶液中加入少量 AgNO3,溶液中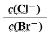 增大
增大
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省高二上期中化学卷(解析版) 题型:选择题
现 有0.1 mol·L-1醋酸溶液10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是
有0.1 mol·L-1醋酸溶液10 mL,加蒸馏水稀释到1 L后,下列变化中正确的是
①电离程度增大 ②c(CH3COOH)增大 ③CH3COO-数目增多 ④c(H+)增大
⑤导电性增强 ⑥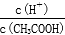 增大 ⑦c(OH-)增大
增大 ⑦c(OH-)增大
A.①②③⑦ B.①③⑤⑥ C.①③⑥⑦ D.②④⑤⑥
查看答案和解析>>
科目:高中化学 来源:2016-2017学年天津市武清区等五区县高二上期中化学卷(解析版) 题型:填空题
汽车尾气是城市空气的主要污染物,如何减少汽车尾气(CO、NOx等)的污染是重要的科学研究课题。
(1)已知:N2(g)+O2(g)═2NO(g) △H1
N2(g)+3H2(g) 2NH3(g) △H2
2NH3(g) △H2
2H2(g)+O2(g)═2H2O(g) △H3
则4NO(g)+4NH3(g)+O2(g)═4N2(g)+6H2O(g)△H=____________(用含△H1、△H2、△H3的式子表达)
(2)汽车尾气中的CO、NOx都需要除去,有人设想按下列反应除去CO;2CO(g)=2C(s)+O2(g)
已知该反应在任何温度下都不能自发进行,因此该设想便不能实现。由此判断该反应的△H________0
目前,在汽车尾气系统中装置催化转化器可以减少CO、NO的污染,其化学反应方程式为____________________。
(3)可用活性炭还原法处理氮氧化物.有关反应的化学方程式为:
C(s)+2NO(g) N2(g)+CO2(g)△H>0
N2(g)+CO2(g)△H>0
某研究小组向密闭容器加入一定量的活性炭和NO,恒温(T1℃)条件下反应,反应进行到不同时间测
C(s)+2NO(g) N2(g)+CO2(g)△H>0
N2(g)+CO2(g)△H>0
得各物质的浓度如下:
浓度/mol•L-1 时间/min | NO | N2 | CO2 |
0 | 0.100 | 0 | 0 |
10 | 0.058 | 0.021 | 0.021 |
20 | 0.040 | 0.030 | 0.030 |
30 | 0.040 | 0.030 | 0.030 |
40 | 0.032 | 0.034 | 0.017 |
则,30min后,改变某一条件,平衡发生了移动,则改变的条件是______________;若升高温度,NO浓度将__________(填“增大”、“不变”或“减小”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com