
【题目】已知反应2H2S+O2=2S↓+2H2O,4NaI+O2+2H2O=4NaOH+2I2和Na2S+I2=2NaI+S↓,下列氧化性大小关系正确的是
A. O2>I2>S B. I2>O2>S C. O2>S>I2 D. S>I2>O2
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:
【题目】NA表示阿伏加德罗常数。下列叙述中正确的是( )
A.标准状况下,2.24L水中含H原子的数目为0.2NA
B.1L 0.1 mol·L-1KNO3溶液里含O原子的数目为0.3NA
C.2.3g钠反应生成Na2O和Na2O2的混合物,转移电子的数目为0.1NA
D.1mol H3O+和1molNH4+中含质子的数目均为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把过氧化钠投入含有HCO3-、Cl-、Mg2+、Na+的水溶液中,离子数目不变的是( )
A. HCO3- B. Cl- C. Mg2+ D. Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学习小组探究溴乙烷的消去反应并验证产物。
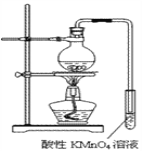
实验过程:组装如图所示装置,检查装置气密性,向烧瓶中注入10mL溴乙烷和15mL饱和氢氧化钠乙醇溶液,微热,观察实验现象。一段时间后,观察到酸性KMnO4溶液颜色褪去。
(1)实验原理:__________________________________。
(2)甲同学认为酸性KMnO4溶液颜色褪去说明溴乙烷发生了消去反应,生成了乙烯;而乙同学却认为甲同学的说法不严谨,请说明原因:_________________________。
(3)丙同学认为只要对实验装置进行适当改进,即可避免对乙烯气体检验的干扰,改进方法:______________________________________________________。
改进实验装置后,再次进行实验,却又发现小试管中溶液颜色褪色不明显。该小组再次查阅资料,对实验进行进一步的改进。
资料一:溴乙烷于55℃时,在饱和氢氧化钠的乙醇溶液中发生取代反应的产物的百分比为99%,而消去反应产物仅为1%。
资料二:溴乙烷发生消去反应比较适宜的反应温度为90℃~110℃,在该范围,温度越高,产生乙烯的速率越快。
资料三:溴乙烷的沸点:38.2℃。
(4)结合资料一、二可知,丙同学改进实验装置后,溶液颜色褪色不明显的原因可能是_______________________________。
(5)结合资料二、三,你认为还应该在实验装置中增加的两种仪器是
①________________________。②___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量金属镁与一定量浓硝酸反应,得到硝酸镁溶液和NO2、NO的混合气体,这些气体与2.52LO2(标准状况)混合后通入水中.所有气体完全被水吸收生成硝酸.若向所得硝酸镁溶液中加入2.5mol/LNaOH溶液至Mg2+恰好完全沉淀,则消耗NaOH溶液的体积是( )
A.45mL
B.180mL
C.90Ml
D.135mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X,Y,Z三种主族元素在周期表中的相对位置如图所示,且X的原子序数为a,下列说法中不正确的是( ) 
A.Y,Z的原子序数之和可能是2a
B.Y的原子序数可能是a﹣17
C.Z的原子序数可能是a+31
D.X,Y,Z一定都是短周期元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com