
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比 ClO-强。25 ℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)Cl2(aq) K1=10-1.2
Cl2(aq)+H2OHClO+H++Cl-K2=10-3.4
HClOH++ClO-Ka=?
其中Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是 ( )。
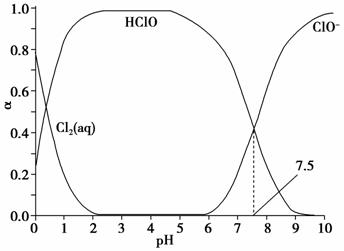
A.Cl2(g)+H2O2H++ClO-+Cl- K=10-10.9
B.在氯处理水体系中,c(HClO)+c(ClO-)=c(H+)-c(OH- )
C.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时差
D.氯处理饮用水时,在夏季的杀菌效果比在冬季好
解析 A项,取图像上两曲线的一个交点(pH=7.5),HClOH++ClO-,Ka=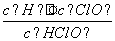 ,由于c(ClO-)=c(HClO),所以Ka=c(H+)=10-7.5,将三个方程式相加可得,Cl2(g)+H2O2H++ClO-+Cl-,则K=K1·K2·Ka=10-4.6×Ka=10-12.1,错误;B项,在氯处理水体系中,根据电荷守恒有c(H+)=c(ClO-)+c(Cl-)+c(OH-),由于Cl2+H2OH++Cl-+HClO,HClOH++ClO-,则c(Cl-)>c(HClO),故c(H+)>c(ClO-)+c(HClO)+c(OH-),错误;C项,由图可知,pH=7.5时的HClO比pH=6.5的HClO的含量少,即pH=7.5时杀菌效果差,正确;D项,由于弱电解质电离是吸热的,夏季温度高,氯的溶解能力变差且HClO易电离,同时也易分解,故夏季杀菌效果比在冬季差,错误。
,由于c(ClO-)=c(HClO),所以Ka=c(H+)=10-7.5,将三个方程式相加可得,Cl2(g)+H2O2H++ClO-+Cl-,则K=K1·K2·Ka=10-4.6×Ka=10-12.1,错误;B项,在氯处理水体系中,根据电荷守恒有c(H+)=c(ClO-)+c(Cl-)+c(OH-),由于Cl2+H2OH++Cl-+HClO,HClOH++ClO-,则c(Cl-)>c(HClO),故c(H+)>c(ClO-)+c(HClO)+c(OH-),错误;C项,由图可知,pH=7.5时的HClO比pH=6.5的HClO的含量少,即pH=7.5时杀菌效果差,正确;D项,由于弱电解质电离是吸热的,夏季温度高,氯的溶解能力变差且HClO易电离,同时也易分解,故夏季杀菌效果比在冬季差,错误。
答案 C


科目:高中化学 来源: 题型:
已知MgO、MgCl2的熔点分别为2800℃、604℃,将MgO、MgCl2加热熔融后通电电解,都可得到金属镁。海水中含有MgCl2,工业上从海水中提取镁,正确的方法是( )
A. 海水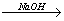 Mg(OH)2
Mg(OH)2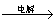 Mg
Mg
B. 海水 MgCl2溶液
MgCl2溶液 MgCl2熔融
MgCl2熔融 Mg
Mg
C. 海水 Mg(OH)2
Mg(OH)2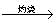 MgO
MgO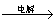 Mg
Mg
D.海水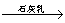 Mg(OH)2
Mg(OH)2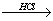 MgCl2溶液
MgCl2溶液  MgCl2熔融
MgCl2熔融 Mg
Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气是氯碱工业的主要产品之一,是一种常用的消毒剂,其消毒原理是与水反应生成了次氯酸:
Cl2+H2OHCl+HClO
次氯酸的强氧化性能杀死水中的病菌(不直接用次氯酸为自来水消毒是因为次氯酸易分解,且毒性较大)。但是由于氯气贮运不方便,且具有一定的危险性,目前正逐渐被其他性能优越的消毒产品所替代。请回答:
(1)氯碱工业生产氯气的化学方程式为_________________________________ _____________________________________________。
(2)84消毒液与氯气相比具有贮运方便等优点,用氯气与烧碱溶液反应制备84消毒液的离子方程式为__________________________________________ _______________________________________________________________。
(3)二氧化氯(ClO2)是目前国际上公认的最新一代的高效、广谱、安全的杀菌、保鲜剂。我国科学家研发了用氯气氧化亚氯酸钠(NaClO2)固体制备二氧化氯的方法,其化学方程式为_________________________________________ _______________________________________________________________________________________________________。
(4)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图所示)。

①下列溶液能吸收Cl2的是____________________________。
A.饱和食盐水 B.饱和Na2SO3溶液
C.饱和NaOH溶液 D.浓硫酸
②能说明Cl2的氧化性强于I2的实验现象是____________________________ ____________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
①氯气的性质活泼,它与氢气混合后立即发生爆炸 ②实验室制取氯气时,为了防止环境污染,多余的氯气可以用氢氧化钙溶液吸收 ③新制氯水的氧化性强于久置氯水的氧化性 ④检验HCl气体中是否混有Cl2,方法是将气体通入硝酸银溶液 ⑤除去HCl气体中的Cl2,可将气体通入饱和食盐水中
A.①②③ B.②③④
C.③ D.③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
关于硅及其化合物的叙述中,错误的是 ( )。
A.硅是良好的半导体材料
B.二氧化硅能与石灰石反应:SiO2+CaCO3 CaSiO3+CO2↑
CaSiO3+CO2↑
C.可以用焦炭还原二氧化硅生产硅:SiO2+2C Si+2CO↑
Si+2CO↑
D.水泥的主要成分是Na2SiO3、CaSiO3和SiO2
查看答案和解析>>
科目:高中化学 来源: 题型:
往100 mL的NaOH溶液中通入CO2充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。通入的CO2的体积V(标准状况)与M的质量(W)的关系如图所示。
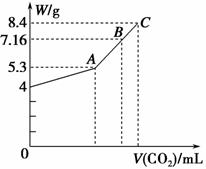
试解答下列问题:
(1)A点时,白色固体M的化学式为________,通入标准状况下的CO2的体积为________ mL。
(2)C点时,白色固体M的化学式为________,通入标准状况下的CO2的体积为________ mL。
(3)B点时M的组成成分为________(用化学式表示),通入的标准状况下的CO2的体积为________ mL。
(4)该NaOH溶液的物质的量浓度为________。
(5)如何检验B点溶液中的阴离子?
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )。
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2CO3溶液和NaHCO3溶液都能跟CaCl2溶液反应得到白色沉淀
③钠在常温下不容易被氧化
④Na2O2可作供氧剂,而Na2O不行
⑤向石蕊试液中加入Na2O2粉末,溶液先变蓝后褪色,并有气泡生成
⑥钠与浓NH4Cl溶液反应,放出的气体中含H2和NH3
A.都正确 B.②③④⑤
C.②⑤⑥ D.④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com