
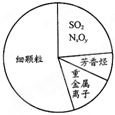
 如图为雾霾的主要成分示意图.下列说法不正确的是( )
如图为雾霾的主要成分示意图.下列说法不正确的是( )| A. | 重金属离子可导致蛋白质变性 | |
| B. | 苯是最简单的芳香烃 | |
| C. | 向空气中大量排放SO2和NxOy都能引起酸雨和光化学烟雾 | |
| D. | 汽车尾气的大量排放是造成雾霾天气的人为因素之一 |
分析 A.芳香烃是指分子中含有苯环结构的碳氢化合物;
B.重金属离子都有较多空轨道易于蛋白质形成配离,使体内的蛋白质凝固及变性;
C.NxOy组成未知,不一定是酸性氧化物;
D.汽车尾气的排放可导致雾霾天气.
解答 解:A.芳香烃是指分子中含有苯环结构的碳氢化合物,最简单的芳香烃是苯,故A正确;
B.重金属离子都有较多空轨道易于蛋白质形成配离子,形成配离子后蛋白质功能就丧失,使体内的蛋白质凝固及变性,故B正确;
C.二氧化硫为酸性氧化物,但NxOy组成未知,不一定是酸性氧化物,故C错误;
D.汽车尾气的排放是雾霾天气的成因之一,故D正确;
故选C.
点评 本题考查了蛋白质、芳香烃、酸性氧化物的定义以及环境污染,涉及知识点广,题目难度不大,熟练掌握物质的性质和概念是解题的关键.


科目:高中化学 来源: 题型:解答题
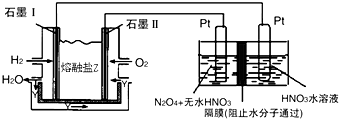
| t/s | 0 | 50 | 100 |
| c(N2O5)/mol•L-1 | 5.0 | 3.5 | 2.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 常温常压下,92g的NO2和N2O4混合气体含有的原子总数为6NA | |
| D. | 17gOH-中含有的质子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 32 g O2占有的体积约为22.4 L | |
| B. | 常温常压下,28g N2含有阿伏加德罗常数个氮气分子 | |
| C. | 在标准状况下,22.4 L水的质量约为18 g | |
| D. | 标准状况下22 g二氧化碳气体与标况下的11.2 L HCl气体含有的分子数不一样多 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
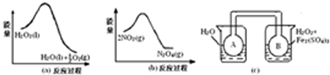
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| KCl | K2SO4 | ZnSO4 | ZnCl2 | |
| (1) | 0.3mol | 0.2mol | 0.1mol | / |
| (2) | 0.1mol | 0.3mol | / | 0.1mol |
| A. | 完全相同 | B. | 完全不同 | C. | 仅c(K+)相同 | D. | 仅c(Cl-)相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com