
| ŹµŃéŠņŗÅ | ¼× | ŅŅ | ±ū |
| ŗĻ½šÖŹĮæ£Ømg£© | 255 | 385 | 459 |
| ±ź×¼×“æöĻĀĘųĢåµÄĢå»ż£ØmL£© | 280 | 336 | 336 |
| A£® | ¼×”¢ŅŅ×éµÄŹµŃéÖŠ£¬ŃĪĖį¾łŹĒ¹żĮæµÄ | B£® | ŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ0.8mol L-1 | ||
| C£® | ŗĻ½šÖŠĆ¾”¢ĀĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1 | D£® | ±ū×éÖŠĀĮµÄĪļÖŹµÄĮæĪŖ0.0045mol |
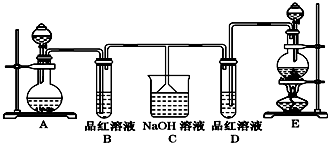
·ÖĪö A£®ŃĪĖįÅØ¶Č”¢Ģå»żŅ»¶Ø£¬¼×ÖŠŗĻ½šÖŹĮæŠ”ÓŚŅŅÖŠŗĻ½šÖŹĮ棬ĒŅ¼×ÖŠÉś³ÉĘųĢåĢå»żŠ”ÓŚŅŅÖŠĘųĢåĢå»ż£¬ĖµĆ÷¼×ÖŠŃĪĖį¹żĮ攢½šŹōĶźČ«·“Ó¦£»øł¾Ż¼×ÖŠ½šŹōÓėĒāĘųµÄĢå»ż¶Ø±Č¹ŲĻµ¼ĘĖćÉś³É336mLĒāĘųŠčŅŖ½šŹōµÄÖŹĮæ£¬Č·¶ØŅŅÖŠŃĪĖįÓė½šŹōŹĒ·ńĒ”ŗĆ·“Ó¦£»
B£®ŅŅ”¢±ūÖŠŃĪĖįĶźČ«£¬æÉŅŌøł¾Ż·“Ӧɜ³ÉĒāĘųĢå»ż¼ĘĖćŃĪĖįµÄĪļÖŹµÄĮæÅØ¶Č£¬øł¾Żn=$\frac{V}{{V}_{m}}$¼ĘĖćĒāĘųµÄĪļÖŹµÄĮ棬øł¾ŻĒāŌŖĖŲŹŲŗćæÉÖŖn£ØHCl£©=2n£ØH2£©£¬¾Ż“Ė¼ĘĖć£»
C£®¼×ÖŠŃĪĖįÓŠŹ£Óą£¬½šŹōĶźČ«·“Ó¦£¬“ĖŹ±Éś³ÉĒāĘų280mL£¬¹ŹæÉŅŌøł¾Ż¼××鏿¾Ż¼ĘĖć½šŹōµÄĪļÖŹµÄĮæÖ®±Č£¬ÉčĆ¾”¢ĀĮµÄĪļÖŹµÄĮæ·Ö±šĪŖxmol”¢ymol£¬øł¾Ż¶žÕßÖŹĮæÖ®ŗĶÓėµē×Ó×ŖŅĘŹŲŗćĮŠ·½³Ģ¼ĘĖćx”¢yµÄÖµ£¬¾Ż“Ė½ā“š£»
D£®øł¾ŻŅŅÖŠĀĮµÄĪļÖŹµÄĮæ¼°ŗĻ½šÖŹĮæ¼ĘĖć³ö±ūÖŠĀĮµÄĪļÖŹµÄĮ森
½ā“š ½ā£ŗA£®ŃĪĖįÅØ”¢Ģå»żŅ»¶Ø£¬¼×ÖŠŗĻ½šÖŹĮæŠ”ÓŚŅŅÖŠŗĻ½šÖŹĮ棬ĒŅ¼×ÖŠÉś³ÉĘųĢåĢå»żŠ”ÓŚŅŅÖŠĘųĢåĢå»ż£¬ĖµĆ÷¼×ÖŠŃĪĖį¹żĮ攢½šŹōĶźČ«·“Ó¦£¬ŅŅÖŠŗĻ½šÖŹĮæŠ”ÓŚ±ūÖŠŗĻ½šÖŹĮ棬ĒŅŅŅ”¢±ūÉś³ÉĘųĢåĢå»żĻąµČ£¬ĖµĆ÷ŅŅ”¢±ūÖŠŃĪĖįĶźČ«·“Ó¦£¬¾Ż¼×æÉÖŖ£¬Éś³É336mLĒāĘųŠčŅŖ½šŹōµÄÖŹĮæĪŖ£ŗ255mg”Į$\frac{336mL}{280mL}$=306mg£¬¹ŹŅŅÖŠ½šŹōÓŠŹ£Óą£¬ŃĪĖį²»×ć£¬¹ŹA“ķĪó£»
B£®ŅŅ”¢±ūÖŠŃĪĖįĶźČ«·“Ó¦£¬æÉŅŌøł¾Ż·“Ӧɜ³ÉĒāĘųĢå»ż¼ĘĖćŃĪĖįµÄĪļÖŹµÄĮæÅØ¶Č£¬ŃĪĖįĶźČ«·“Ӧɜ³ÉĒāĘų336mL£¬ĒāĘųµÄĪļÖŹµÄĮæĪŖ£ŗ$\frac{0.336L}{22.4L/mol}$=0.015mol£¬øł¾ŻĒāŌŖĖŲŹŲŗćæÉÖŖ£ŗn£ØHCl£©=2n£ØH2£©=2”Į0.015mol=0.03mol£¬¹ŹŃĪĖįµÄĪļÖŹµÄĮæÅضČĪŖ£ŗ$\frac{0.03mol}{0.03L}$=1mol/L£¬¹ŹB“ķĪó£»
C£®¼×ÖŠŃĪĖįÓŠŹ£Óą£¬½šŹōĶźČ«·“Ó¦£¬“ĖŹ±Éś³ÉĒāĘų280mL£¬¹ŹæÉŅŌøł¾Ż¼××鏿¾Ż¼ĘĖć½šŹōµÄĪļÖŹµÄĮæÖ®±Č£¬ÉčĆ¾”¢ĀĮµÄĪļÖŹµÄĮæ·Ö±šĪŖxmol”¢ymol£¬øł¾Ż¶žÕßÖŹĮææÉÖŖ£ŗ¢Ł24x+27y=0.255£¬øł¾Żµē×Ó×ŖŅĘŹŲŗćÓŠ£ŗ¢Ś2x+3y=$\frac{0.28L}{22.4L/mol}$”Į2£¬øł¾Ż¢Ł¢ŚĮŖĮ¢½āµĆ£ŗx=0.005”¢y=0.005£¬ĖłŅŌŗĻ½šÖŠĆ¾ÓėĀĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ£ŗ0.005mol£ŗ0.005mol=1£ŗ1£¬¹ŹCÕżČ·£»
D£®¼×ÖŠ255gŗĻ½šÖŠŗ¬ÓŠ0.005molĀĮ£¬Ōņ±ūÖŠ459gŗĻ½šÖŠŗ¬ÓŠĀĮµÄĪļÖŹµÄĮæĪŖ£ŗ0.005mol”Į$\frac{459g}{385g}$=0.006mol£¬¹ŹD“ķĪó£»
¹ŹŃ”C£®
µćĘĄ ±¾Ģāæ¼²é»ģŗĻĪļ·“Ó¦µÄ¼ĘĖć£¬ĢāÄæÄѶČÖŠµČ£¬øł¾Ż±ķÖŠŹż¾Ż¹ŲĻµÅŠ¶Ļ·“Ó¦µÄ¹żĮæĪŹĢāĪŖ½ā“š¹Ų¼ü£¬×¢ŅāŹģĮ·ÕĘĪÕĪļÖŹµÄĮæÓėĦ¶ūÖŹĮ攢ĘųĢåĦ¶ūĢå»żµČÖ®¼äµÄ¹ŲĻµ£¬ŹŌĢāÅąŃųĮĖѧɜµÄ»Æѧ¼ĘĖćÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ħ¶ūŹĒ°ŃĪļÖŹµÄÖŹĮæŗĶĪ¢¹ŪĮ£×ÓŹżĮŖĻµĘšĄ“µÄŅ»øö»ł±¾ĪļĄķĮæ | |
| B£® | 1Ħ¶ūH2SO4µÄÖŹĮæĪŖ98g/mol | |
| C£® | ¹ś¼ŹÉĻ¹ę¶Ø£¬0.012 kg Ģ¼Ō×ÓĖłŗ¬ÓŠµÄĢ¼Ō×ÓŹżÄæĪŖ 1 mol | |
| D£® | 1Ħ¶ūĒāĘų·Ö×ÓæÉŅŌ±ķŹ¾ĪŖ1mol H2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | m=4 R2+ŹĒ»¹Ō¼Į | B£® | m=n R3+ŹĒŃõ»Æ²śĪļ | ||
| C£® | m=2 R2+ŹĒŃõ»Æ¼Į | D£® | m=y R3+ŹĒ»¹Ō²śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 3 mL | B£® | 7.5 mL | C£® | 15 mL | D£® | 22.5 mL |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | Ńõ»Æ¼ĮŹĒCl2 | |
| B£® | Ńõ»Æ¼ĮÓė»¹Ō¼ĮµÄĪļÖŹµÄĮæÖ®±ČĪŖ3£ŗ8 | |
| C£® | ĆæÉś³É1molN2£¬×ŖŅĘ3molµē×Ó | |
| D£® | ±»Ńõ»ÆÓėĪ“±»Ńõ»ÆµÄNH3ĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 2Na2O2+2Mn2O7”ś4NaMnO4+O2”ü | B£® | 2Na2O2+P2O3”śNa4P2O7 | ||
| C£® | 2Na2O2+2 N2O3”śNaNO2+O2”ü | D£® | 2 Na2O2+2 N2O5”ś4NaNO3+O2”ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
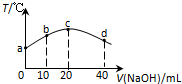 ³£ĪĀĻĀ£¬ČōĶł20mL 0.01mol•L-1 HNO2£ØČõĖį£©ČÜŅŗÖŠÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄÉÕ¼īČÜŅŗ£¬²āµĆ»ģŗĻČÜŅŗµÄĪĀ¶Č±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©
³£ĪĀĻĀ£¬ČōĶł20mL 0.01mol•L-1 HNO2£ØČõĖį£©ČÜŅŗÖŠÖšµĪ¼ÓČėŅ»¶ØÅØ¶ČµÄÉÕ¼īČÜŅŗ£¬²āµĆ»ģŗĻČÜŅŗµÄĪĀ¶Č±ä»ÆČēĶ¼ĖłŹ¾£¬ĻĀĮŠÓŠ¹ŲĖµ·Ø²»ÕżČ·µÄŹĒ£Ø””””£©| A£® | HNO2µÄµēĄėĘ½ŗā³£Źż£ŗcµć£¾bµć | |
| B£® | Ėł¼ÓÉÕ¼īČÜŅŗPH=12£¬cµćĖ®µÄĄė×Ó»ż³£ŹżKW=10-14 | |
| C£® | cµć»ģŗĻČÜŅŗÖŠ£ŗc£ØOH-£©£¾c£ØHNO2£© | |
| D£® | dµć»ģŗĻČÜŅŗÖŠ£ŗc£ØNa+£©£¾c£ØOH-£©£¾c£ØNO2-£©£¾c£ØH+£© |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | c£ØOH-£©/c£ØH+£©=10-12µÄČÜŅŗÖŠ£ŗK+”¢Ba2+”¢Br-”¢Cl- | |
| B£® | 0.1mol•L”„1NaHC2O4ČÜŅŗÖŠ£ŗK+”¢Ba2+”¢OH-”¢Cl- | |
| C£® | pH=7µÄČÜŅŗÖŠ£ŗFe3+”¢Na+”¢Cl-”¢NO3- | |
| D£® | ŗ¬ÓŠ“óĮæClO-µÄČÜŅŗÖŠ£ŗK+”¢OH-”¢I-”¢SO32- |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com