
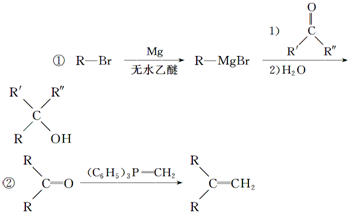
 ��R��ʾ������R��R��ʾ�������⣩
��R��ʾ������R��R��ʾ�������⣩ ��
��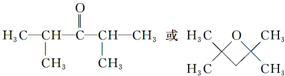 ����дһ�֣���
����дһ�֣���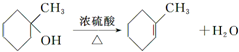 ��
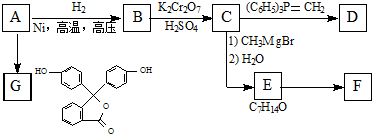
��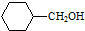 �ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�H2C�TCH2+CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH��
�ĺϳ�·������ͼ�����Լ����ã����ϳ�·������ͼʾ�����£�H2C�TCH2+CH3CH2Br$��_{��}^{NaOH��Һ}$CH3CH2OH�� ���� ������A������ʽΪC6H6O����һ���л�����ԭ�ϣ��ڿ������ױ����������G�Ľṹ��֪��A�Ľṹ��ʽΪ�� ��A�����������ӳɷ�Ӧ����BΪ��
��A�����������ӳɷ�Ӧ����BΪ��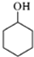 ��B���ظ���������õ�C��C������Ϣ���еķ�Ӧ�õ�E�����E�ķ���ʽ��֪��CΪ
��B���ظ���������õ�C��C������Ϣ���еķ�Ӧ�õ�E�����E�ķ���ʽ��֪��CΪ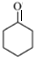 ��EΪ
��EΪ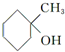 ��C������Ϣ�ڵķ�Ӧ�õ�DΪ��
��C������Ϣ�ڵķ�Ӧ�õ�DΪ��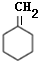 ��E��Ӧ����F��F��D��Ϊͬ���칹�壬����E������ȥ��Ӧ����F����F�Ľṹ��ʽΪ��
��E��Ӧ����F��F��D��Ϊͬ���칹�壬����E������ȥ��Ӧ����F����F�Ľṹ��ʽΪ��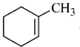 ����5���б��������������ӳɷ�Ӧ�õ�����������������HBr����ȡ����Ӧ�õ�
����5���б��������������ӳɷ�Ӧ�õ�����������������HBr����ȡ����Ӧ�õ�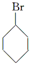 ��
�� ��Mg/��ˮ���ѷ�Ӧ�õ�
��Mg/��ˮ���ѷ�Ӧ�õ�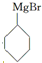 ������HCHO��Ӧ��ˮ��õ�
������HCHO��Ӧ��ˮ��õ�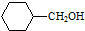 ���ݴ˽��
���ݴ˽��
��� �⣺������A������ʽΪC6H6O����һ���л�����ԭ�ϣ��ڿ������ױ����������G�Ľṹ��֪��A�Ľṹ��ʽΪ�� ��A�����������ӳɷ�Ӧ����BΪ��
��A�����������ӳɷ�Ӧ����BΪ�� ��B���ظ���������õ�C��C������Ϣ���еķ�Ӧ�õ�E�����E�ķ���ʽ��֪��CΪ
��B���ظ���������õ�C��C������Ϣ���еķ�Ӧ�õ�E�����E�ķ���ʽ��֪��CΪ ��EΪ
��EΪ ��C������Ϣ�ڵķ�Ӧ�õ�DΪ��
��C������Ϣ�ڵķ�Ӧ�õ�DΪ�� ��E��Ӧ����F��F��D��Ϊͬ���칹�壬����E������ȥ��Ӧ����F����F�Ľṹ��ʽΪ��
��E��Ӧ����F��F��D��Ϊͬ���칹�壬����E������ȥ��Ӧ����F����F�Ľṹ��ʽΪ�� ��
��
��1��������������֪��A�Ľṹ��ʽΪ�� ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��2����G�Ľṹ��ʽ��֪��G�ķ���ʽΪC20H14O4���ʴ�Ϊ��C20H14O4��
��3��ij��������E�� ����ͬ���칹�壬�ҷ�����ֻ�����ֲ�ͬ��ѧ�������⣬�Գ��Ըߣ��û�����Ľṹ��ʽ��
����ͬ���칹�壬�ҷ�����ֻ�����ֲ�ͬ��ѧ�������⣬�Գ��Ըߣ��û�����Ľṹ��ʽ��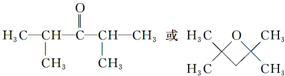 ��
��
�ʴ�Ϊ��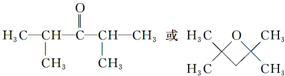 ��
��
��4����ӦE��F�Ļ�ѧ����ʽ�� ��
��
�ʴ�Ϊ�� ��
��
��5�����������������ӳɷ�Ӧ�õ�����������������HBr����ȡ����Ӧ�õ� ��
�� ��Mg/��ˮ���ѷ�Ӧ�õ�
��Mg/��ˮ���ѷ�Ӧ�õ� ������HCHO��Ӧ��ˮ��õ�
������HCHO��Ӧ��ˮ��õ�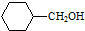 ���ϳ�·������ͼΪ��
���ϳ�·������ͼΪ��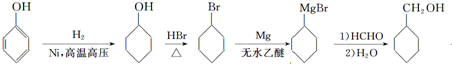 ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л�����ƶ���ϳɣ���Ҫѧ���Ը������Ϣ�������ã��ܽϺõĿ���ѧ����ȡ��Ϣ������֪ʶǨ������������������ע�����G�Ľṹ��A�ķ���ʽ�ж�A�Ľṹ��ʽ���ٽ�Ϸ�Ӧ���������ƶϣ��Ǹ߿��������ͣ��Ѷ��еȣ�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����淴Ӧ���ʶ������� | B�� | SO2��O2��SO3��Ũ����� | ||
| C�� | SO2��O2��SO3�������й��� | D�� | SO2��O2��SO3��Ũ�Ⱦ����ٱ仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��1��ʵ���ҿ�����ͼװ����ȡ��Ȳͼ��A�ܵ������ǵ���ˮ��ĸ߶������Ʒ�Ӧ�ķ�����ֹͣ����ȡ��Ȳ�Ļ�ѧ��Ӧ����ʽΪCaC2+2H2O��C2H2��+Ca��OH��2
��1��ʵ���ҿ�����ͼװ����ȡ��Ȳͼ��A�ܵ������ǵ���ˮ��ĸ߶������Ʒ�Ӧ�ķ�����ֹͣ����ȡ��Ȳ�Ļ�ѧ��Ӧ����ʽΪCaC2+2H2O��C2H2��+Ca��OH��2�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com