
【题目】如图所示中学化学中常见物质的实验转化过程,部分物质和反应条件略去。
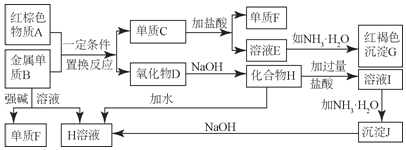
(1)写出F的化学式______;写出物质A的一种用途______;
(2)写出单质B与强碱溶液反应的离子方程式______,写出沉淀J生成H溶液的离子方程式______;
(3)溶液E中加入氨水时,先生成白色沉淀L,写出生成L的离子方程式______;
(4)溶液I中所含金属离子是______。
【答案】![]() 作油漆颜料,炼铁等
作油漆颜料,炼铁等 ![]()
![]()
![]()
![]() 、
、![]()
【解析】
金属B与强碱反应得到单质F与H,则B为Al、F为![]() ,H为偏铝酸盐,G为红褐色沉淀,则G为
,H为偏铝酸盐,G为红褐色沉淀,则G为![]() ,红棕色物质A与金属Al发生置换反应生成单质C与氧化物D,则A为
,红棕色物质A与金属Al发生置换反应生成单质C与氧化物D,则A为![]() 、C为Fe、D为
、C为Fe、D为![]() ,由转化关系可知,E为
,由转化关系可知,E为![]() ,H为
,H为![]() ,溶液I为NaCl、HCl、
,溶液I为NaCl、HCl、![]() 混合物,J为
混合物,J为![]() ,据此解答。
,据此解答。
(1)由上述分析可知,单质F的化学式是![]() ,物质A为
,物质A为![]() ,可以用作油漆颜料,炼铁等,
,可以用作油漆颜料,炼铁等,
故答案为:![]() ;用作油漆颜料,炼铁等;
;用作油漆颜料,炼铁等;
(2)单质Al与强碱溶液反应的离子方程式:![]() ,由沉淀J生成H溶液的离子方程式为:
,由沉淀J生成H溶液的离子方程式为:![]() ,
,
故答案为:![]() ;
;![]() ;
;
(3)溶液![]() 中加入氨水时,先生成白色沉淀L为
中加入氨水时,先生成白色沉淀L为![]() ,离子方程式:
,离子方程式:![]() ,
,
故答案为:![]() ;
;
(4)溶液I为NaCl、HCl、![]() 混合物,所含金属离子是
混合物,所含金属离子是![]() 、
、![]() ,
,
故答案为:![]() 、
、![]() 。
。


科目:高中化学 来源: 题型:
【题目】工业合成氨的反应为N2(g)+3H2(g)![]() 2NH3(g),已知下列化学键的键能:
2NH3(g),已知下列化学键的键能:
化学键 | 键能kJ/mol |
H-H | 436 |
N-H | 391 |
N | 946 |
下列说法正确的是
A. 该反应为吸热反应B. 该反应中反应物的总能量高于生成物的总能量
C. 反应热ΔH=92 kJ·mol-1D. 生成1 mol NH3放出92 kJ热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水合肼(N2H4·H2O)是无色,具有强还原性的液体,易溶于水,沸点约为118℃,实验室可用如下图所示实验装置制取水合肼。

(1)仪器X的名称是:__________。
(2)制取N2H4·H2O反应中还有Na2CO3、NaCl生成。写出反应的化学方程式:__________。
(3)反应时应逐滴滴加NaClO溶液,且NaClO溶液不能过量,原因是__________。
(4)某实验小组用如下实验测定某溶液中N2H4·H2O的含量(g·L1):
步骤1:准确量取溶液25.00 mL,向其中加入过量的浓度为0.5000 mol·L-1的I2溶液20.00 mL、一定量的H2SO4和NaHCO3,充分反应;
步骤2:向步骤1反应后的溶液中滴加少量淀粉溶液,用0.5000 mol·L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液16.00 mL。
测定过程中的反应如下:
N2H4·H2O+H2SO4+NaHCO3+I2-N2↑+CO2↑+Na2SO4+NaI+H2O(未配平)
2Na2S2O3+I2=Na2S4O6+2NaI
计算溶液中N2H4·H2O的含量(g·L1),写出计算过程_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产中常用MnS作沉淀剂除去工业废水中的Cu2+:Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq)下列有关叙述中正确的是( )
CuS(s)+Mn2+(aq)下列有关叙述中正确的是( )
①MnS的Ksp大于CuS的Ksp ②达到平衡时c(Mn2+)=c(Cu2+) ③溶液中加入少量Na2S固体后,溶液中c(Cu2+)、c(Mn2+)保持不变 ④该反应平衡常数K=
A. ①④ B. ②③
C. ①②③ D. ②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有Ⅰ~Ⅳ四个体积均为 0.5 L 的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入 HCl 和 O2(如下表),加入催化剂发生反应 4HCl(g)+O2(g) ![]() 2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
2Cl2(g)+2H2O(g) ΔH,HCl 的平衡转化率(α)与 Z 和温度(T)的关系如图 所示。下列说法正确的是
容器 | 起始时 | ||
t/℃ | n(HCl)·mol-1 | Z | |
I | 300 | 0.25 | a |
II | 300 | 0.25 | b |
III | 300 | 0.25 | 4 |
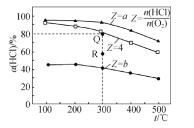
A.ΔH<0,b<4<a
B.300 ℃该反应的平衡常数的值为 64
C.容器Ⅲ某时刻处在 R 点,则 R 点的 v 正>v 逆,压强:p(R)>p(Q)
D.若起始时,在容器Ⅳ中充入 0.25 mol Cl2 和 0.25 mol H2O(g),300 ℃达平衡时容器中 c(HCl)=0.1 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某![]() 样品中含有
样品中含有![]() 和
和![]() 杂质,现欲制取纯净的
杂质,现欲制取纯净的![]() ,某同学设计如图的实验方案。请回答下列问题:
,某同学设计如图的实验方案。请回答下列问题:

(1)操作Ⅰ的名称是______,在该操作中用到的玻璃仪器除了有烧杯、玻璃棒,还有______
(2)沉淀A的成分是______![]() 填化学式
填化学式![]() ,写出第③步反应中铝元素转化的离子方程式______
,写出第③步反应中铝元素转化的离子方程式______
(3)写出证明滤液B中![]() 已沉淀完全的实验方法______
已沉淀完全的实验方法______
(4)不改变上述流程图的结构,将“①过量盐酸”“②过量NaOH”交换位置,则“③过量![]() ”应改为_____,写出此方案下生成沉淀B的离子方程式______
”应改为_____,写出此方案下生成沉淀B的离子方程式______
(5)为了得到更加纯净的![]() ,过滤后需要进行操作步骤是______
,过滤后需要进行操作步骤是______
(6)写出工业由氧化铝冶炼铝的化学方程式______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】影响化学反应速率的因素很多,某课外兴趣小组用实验方法进行探究。
(1)取等物质的量浓度、等体积的H2O2溶液分别进行H2O2的分解实验,实验报告如下表所示(现象和结论略)。

①实验1、2研究的是__________对H2O2分解速率的影响。
②实验2、3的目的是_______________对H2O2分解速率的影响。
(2)查文献可知,Cu2+对H2O2分解也有催化作用,为比较Fe3+、Cu2+对H2O2分解的催化效果,该小组的同学分别设计了如图甲、乙所示的实验。回答相关问题:

①定性如图甲可通过观察_______,定性比较得出结论。有同学提出将CuSO4溶液改为CuCl2溶液更合理,其理由是_________。
②定量如图乙所示,实验时以收集到40 mL气体为准,忽略其他可能影响实验的因素,实验中需要测量的数据是__________。
(3)酸性高锰酸钾溶液和草酸溶液可发生反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+8H2O+10CO2↑,实验时发现开始反应速率较慢,溶液褪色不明显,但一段时间后突然褪色,反应速率明显加快。对此展开讨论:
①某同学认为KMnO4与H2C2O4的反应是______热反应,导致_______________;
②从影响化学反应速率的因素看,你认为还可能是________的影响。要证明你的猜想,实验方案是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】偏二甲肼![]() 为
为![]() 价
价![]() 与
与![]() 是常用的火箭推进剂,发生的化学反应如下:
是常用的火箭推进剂,发生的化学反应如下:![]()
![]() ,下列说法不正确的是
,下列说法不正确的是 ![]()
![]()
A.该反应在任何情况下都能自发进行
B.![]() 含有
含有![]() 共价键
共价键
C.反应中,氧化产物为![]() ,还原产物为
,还原产物为![]()
D.反应中,生成![]() 时,转移
时,转移![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A2 + 3B2(?)![]() 2AB3(g)中,AB3的百分含量(w)与温度和压强的关系如图所示。下列说法正确的是( )
2AB3(g)中,AB3的百分含量(w)与温度和压强的关系如图所示。下列说法正确的是( )
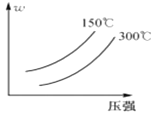
A.该反应为吸热反应
B.反应物B2为气体
C.升高温度,逆反应速率减慢
D.增大压强,A2转化率减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com